时间:2025-06-26 03:14:56
1、选择题 对于平衡体系2SO2(g) + O2(g)  2SO3(g);ΔH<0.下列结论中正确的是
2SO3(g);ΔH<0.下列结论中正确的是
A.若温度不变,将容器的体积增大一倍,此时的SO2浓度变为原来的0.48倍
B.若平衡时SO2、O2的转化率相等,说明反应开始时,两者的物质的量之比为2:1
C.若从平衡体系中分离出SO3,则有利于提高SO2的转化率和加快正反应速率
D.平衡状态时SO2、O2、SO3的物质的量之比一定为2:1:2
参考答案:B
本题解析:略
本题难度:简单
2、简答题 在一定温度下,将4mol?SO2与2molO2放入4L的密闭容器中,在一定条件下反应,10分钟时达到平衡:2SO2+O2?2SO3测得平衡时混合物总物质的量为5mol,求:
(1)10分钟时O2的反应速率为______mol/(L?min)
(2)平衡时SO2的转化率______
(3)该反应的平衡常数为______.
参考答案:在一定温度下,将4mol?SO2与2molO2放入4L的密闭容器中,c(SO2)=1mol/L,c(O2)=0.5mol/L,
设转化的氧气的物质的量为x,则
? 2SO2+O2?2SO3
开始? 4? 2? 0
转化? 2x? x? 2x
平衡? 4-2x 2-x? 2x
平衡时混合物总物质的量为5mol,
所以4-2x+2-x+2x=5,解得x=1mol,
(1)10分钟时O2的反应速率为1mol4L10min=0.025mol/(L.nim),故答案为:0.025;
(2)平衡时SO2的转化率为2mol4mol×100%=50%,故答案为:50%;
(3)平衡时c(SO2)=0.5mol/L,c(O2)=0.25mol/L,c(SO3)=0.5mol/L,
反应的平衡常数K=c(SO3)2c(O2)×c(SO2)2=(0.5mol/L)2(0.5mol/L)2×0.25mol/L=4L/mol,故答案为:4L/mol.
本题解析:
本题难度:一般
3、选择题 已知:t℃下的某一气态平衡体系中含有X(g)、Y(g)、Z(g)、W(g)四种物质,此温度下发生反应的平衡常数表达式为: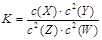 ,有关该平衡的说法中正确的是(?)
,有关该平衡的说法中正确的是(?)
A.升高温度,平衡常数K变大
B.增大压强,W(g)物质的量分数变小
C.升温,若混合气体的平均相对分子质量变小,则逆反应放热
D.增大Z浓度,平衡向正反应方向移动
参考答案:BD
本题解析:
正确答案:BD
A.不正确,本反应不知是吸热还是放热反应,升高温度,平衡常数K 无法确定变大变小;
B.正确,该反应为气体体积缩小的反应,增大压强,W(g)物质的量分数变小
C.不正确,升温,若混合气体的平均相对分子质量变小,则平衡逆向移动,逆反应吸热
D.正确,Z是反应物,增大Z浓度,平衡向正反应方向移动
本题难度:一般
4、计算题 在5 L的密闭容器中充入2 mol A气体和1 mol B气体,在一定条件下发生反应:2A(g)+B(g) 2C(g),10min后达平衡时,在相同温度
2C(g),10min后达平衡时,在相同温度 下测得容器内混合气体的物质的量是反应前的5/6,试计算
下测得容器内混合气体的物质的量是反应前的5/6,试计算
①A的转化率
②平衡常数K
③10min内生成物C的反应速率
参考答案:
本题解析:略
本题难度:一般
5、选择题 在一定温度下,可逆反应A(气)+3B(气)  2C(气)达到平衡的标志是(? )?
2C(气)达到平衡的标志是(? )?
A.A、B、C的分子数比为1:3:2?
B.A、B、C的浓度相等
C.C生成的速率与C分解的速率相等?
D.单位时间生成n mol A,同时生成3n mol B
参考答案:C
本题解析: A达平衡时,A、B、C三种物质的分子数之比可能是1:3:2,也可能不是1:3:2,与反应开始时加入的A、B物质的量及物质转化率有关,故A错误;
B、在一定条件下的可逆反应里,达到平衡状态时,反应混合物中各组成成分的浓度保持不变而不是相等所以B选项是错误的D、生成n mol A,同时生成3n mo1B,都表示逆反应速率,无论反应是否达到平衡,这个关系总是成立的,反应方向一致,故D错误;故选C.
本题难度:一般