时间:2025-06-26 03:11:40
1、实验题 测定1 mol氧气在标准状况下所占体积的实验操作的步骤如下:
①按下图装配实验装置。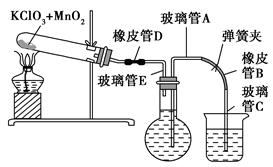
②洗净试管然后充分干燥。
③向500 mL烧瓶里装满水,向500 mL烧杯里加入少量水,把连接烧瓶和烧杯的玻璃管A、橡皮管B和玻璃管C中也装满水,在中间不要留下气泡,然后用弹簧夹把橡皮管B夹紧。
④称得试管的质量为14.45 g,往试管里加入KClO3和MnO2的混合物,再称其质量为15.95 g。
⑤打开弹簧夹,把烧杯举起使烧瓶和烧杯中的水面一致,再关闭弹簧夹,然后把烧杯中的水倒掉。
⑥打开弹簧夹,加热试管的混合物到不再产生气体,即水不再流向烧杯时为止。
⑦反应完毕后把装置冷却到室温。
⑧调节烧杯的高度使烧瓶和烧杯中的水面一致,然后再关闭弹簧夹。
⑨用500 mL量筒测量烧杯里水的体积为285.0 mL,把它换算为标准状况下氧气的体积为279.7 mL。
⑩再称量冷却后试管的质量为15.55 g。
(1)在操作⑦中,装置冷却时,玻璃管C的出口一直要在烧杯的水中,不能离开水面,其理由是 。
(2)简述操作⑧的必要性,即为什么要调节烧杯的高度,使烧瓶和烧杯中的水面一致? 。
(3)标准状况下,1 mol氧气所占的体积(保留小数后两位)为 L;混合物中MnO2的质量分数为 。
2、填空题 (1)44gCO2的物质的量为______;标准状况下其所占的体积为______;
(2)500mLNaOH溶液中含4gNaOH,则该溶液中c(NaOH)为______;
(3)0.4mol/L的Al2(SO4)3溶液200mL,则该溶液中c(SO
3、填空题 (10分)下图为实验室某浓盐酸试剂瓶标签上的有关数据,
试根据标签上的有关数 据回答下列问题:
(1)该盐酸中HCl的物质的量浓度为 △ mol?L
4、选择题 标准状况下,32g某气体的分子数与22 g CO2的分子数相同,则该气体的摩尔质量为
A.32
B.64 g/ mol
C.32g/ mol
D.64
5、简答题 把2mol/LCuCl2溶液和2mol/L盐酸等体积混合(假设混合后溶液体积等于混合前两种溶液的体积之和).请计算:
(1)混合液中CuCl2和盐酸的物质的量浓度;______
(2)混合液中H+、Cu2+、Cl-的物质的量浓度;______
(3)向溶液中加入足量的铁粉,经足够长的时间后,铁粉有剩余.此时溶液中FeCl2的物质的量浓度.______.