ʱ��:2025-06-26 02:34:06
1��ʵ���� ��11�֣�ij�о���ѧϰС��Ϊ֤��2Fe3+ + 2I-  ?2Fe2+ + I2Ϊ���淴Ӧ������Ӧ����һ�����ȣ���������¼��ַ�������֪FeF63-��һ����ɫ���ȶ��������ӡ�
?2Fe2+ + I2Ϊ���淴Ӧ������Ӧ����һ�����ȣ���������¼��ַ�������֪FeF63-��һ����ɫ���ȶ��������ӡ�
��Ҫ��ش��������⡣
�����ף�
ȡ5mL 0.1mol/L KI��Һ���μ�2ml 0.1mol/L ��FeCl3��Һ���ټ�������2mL CCl4����������á��ֲ㣬��ȡ�ϲ���Һ���μ�KSCN��Һ��
��1����������֤���÷�ӦΪ���淴Ӧ��������?��
��2����ͬѧ��Ϊ�÷�����Ʋ������ܣ���ʹ�÷�ӦΪ�����淴ӦҲ���ܳ�������������ԭ����?��
�����ң�
ȡ5mL 0.1mol/L KI��Һ���μ�2ml 0.1mol/L ��FeCl3��Һ����Һ���ػ�ɫ��������Һ�еμ�NH4F��Һ��������?������֤���÷�ӦΪ���淴Ӧ������Ͳ����������ԭ��?��
��������
�����ͼԭ���װ�ã���ͨ���������ƣ�ָ������ƫת��ע������������ָ������ƫ���Դ������������ʱ����е����ƶ�����С����������Ϊ�㡣
��ָ���������������ձ��м���1mol/L FeCl2��Һ�����۲쵽���������Ƶ�ָ����?����ƫת��������ҡ����ƶ������������жϸ÷�ӦΪ���淴Ӧ����ʱ����ʯī�缫�ϵĵ缫��ӦʽΪ?��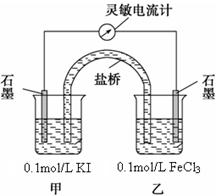
�ο��𰸣���1���²㣨CCl4�㣩��Һ���Ϻ�ɫ�����ϲ���Һ�еμ�KSCN����Һ��Ѫ��ɫ����2�֣�
��2�������в����е�Fe2+���ӱ�������������������2�֣�
�����ң���Һ���ػ�ɫ��Ϊ��ɫ�����dz������1�֣�
Fe3+��F-���������ɫ��FeF63-����ʹ2Fe3+ + 2I-  ?2Fe2+ + I2ƽ�⳯�淴Ӧ�����ƶ�?��2�֣�
?2Fe2+ + I2ƽ�⳯�淴Ӧ�����ƶ�?��2�֣�
����������2�֣���I2 +2e- = 2I-��2�֣�
�����������1������ʵ�����ݿ�֪�⻯���ǹ����ģ�����Ӧ�ǿ��淴Ӧ������Һ��һ�����������ӣ�ͬʱҲ�������ɵ��ʵ⡣���Կ���ͨ�����������Ӻ͵��ʵ���֤����
��2����Ϊ�����Ӻ����������ڿ�����Ҳ���Ա������������ɵ��ʵ�������ӣ����Է������Ǻ����ܡ�
��3�������������������ƽ���Ӱ������֤����ΪFe3+��F-���������ɫ��FeF63-����ʹ2Fe3+ + 2I-  ?2Fe2+ + I2ƽ�⳯�淴Ӧ�����ƶ���������Һ��ɫ���dz��
?2Fe2+ + I2ƽ�⳯�淴Ӧ�����ƶ���������Һ��ɫ���dz��
��4����ԭ����и�����ʧȥ���ӵģ�������ʧȥ���ӣ����Ե����ǴӼ׳������ҳأ����Ե����Ƶ�ָ������ƫת��
�����Ѷȣ�һ��
2��ѡ���� T��ʱ��A�����B���巴Ӧ����C���塣��Ӧ������A��B��CŨ�ȱ仯����ͼ����ʾ�������������������䣬�¶ȷֱ�ΪT1��T2ʱ��B�����������ʱ��Ĺ�ϵ����ͼ����ʾ�������н�����ȷ����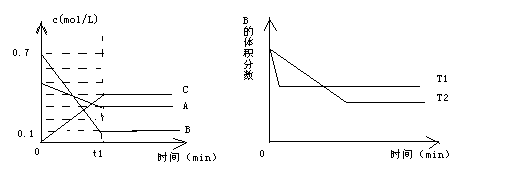
��?��
A��t1minʱ�����������������䣬����ѹǿ��ƽ�����淴Ӧ�����ƶ�?
B��t1minʱ������������������䣬ͨ������ϡ�����壬ƽ�����淴Ӧ�����ƶ�
C��������������ʱ�������¶ȣ������淴Ӧ���ʾ�������A��ת���ʼ�С
D�� T��ʱ������ͬ�����У�����1.0mol/L A��1.4mol/L B��ʼ��Ӧ���ﵽƽ���C��Ũ�ȵ���0.8mol/L
�ο��𰸣�C
�������������ͼ���֪��ƽ��ʱAB�����ʵ���Ũ�ȷֱ������0.5mol/L��0.3mol/L��0.2mol/L��0.7mol/L��0.1mol/L��0.6mol/L��C��Ũ��������0.4mol/L�����Ը÷�Ӧ�ķ���ʽΪA��3B 2C�����÷�Ӧ�������С�ķ�Ӧ����������ѹǿƽ��������Ӧ�����ƶ���A����ȷ��B�������ݻ����䣬ABC��Ũ�Ȳ��䣬ƽ�ⲻ�ƶ���B����ȷ������ͼ���ҿ�֪���¶�ΪT2ʱ���ȴﵽƽ�⣬˵���¶���T2����T1�����¶ȸߣ�B�����������˵�������¶ȣ�ƽ�����淴Ӧ�����ƶ�����������Ӧ�Ƿ��ȷ�Ӧ��ѡ��C��ȷ�����ڷ�Ӧ�������С�ģ�ѡ��D���൱������ѹǿ������ƽ��ʱC��Ũ��Ӧ�ô���0.8mol/L��ѡ��D����ȷ����ѡC��
2C�����÷�Ӧ�������С�ķ�Ӧ����������ѹǿƽ��������Ӧ�����ƶ���A����ȷ��B�������ݻ����䣬ABC��Ũ�Ȳ��䣬ƽ�ⲻ�ƶ���B����ȷ������ͼ���ҿ�֪���¶�ΪT2ʱ���ȴﵽƽ�⣬˵���¶���T2����T1�����¶ȸߣ�B�����������˵�������¶ȣ�ƽ�����淴Ӧ�����ƶ�����������Ӧ�Ƿ��ȷ�Ӧ��ѡ��C��ȷ�����ڷ�Ӧ�������С�ģ�ѡ��D���൱������ѹǿ������ƽ��ʱC��Ũ��Ӧ�ô���0.8mol/L��ѡ��D����ȷ����ѡC��
�����Ѷȣ�һ��
3������� (18��)��Դ�Ŀ����������ǵ�ǰ��ѧ�о�����Ҫ���⡣
(1)���ö�������(CeO2)��̫����������ǰʵ�����±��Ϊ���Ĺ��̣�
mCeO2 ?(m-x)CeO2
?(m-x)CeO2 xCe+xO2
xCe+xO2
(m-x)CeO2 xCe+xH2O+xCO2
xCe+xH2O+xCO2 mCeO2+xH2+xCO
mCeO2+xH2+xCO
�������̵��ܷ�Ӧ��?,�÷�Ӧ��̫����ת��Ϊ?��
(2)CO��O2��KOH��Һ���ɵ�ȼ�ϵ�صĸ����缫��ӦʽΪ?���õ�ط�Ӧ�ɻ��K2CO3��Һ��ij�¶���0.5mol L-1 K2CO3��Һ��pH=12��������CO32-�ĵڶ���ˮ�⣬��CO32- +H2O
L-1 K2CO3��Һ��pH=12��������CO32-�ĵڶ���ˮ�⣬��CO32- +H2O HCO3-+OH-��ƽ�ⳣ��Kh= ?��
HCO3-+OH-��ƽ�ⳣ��Kh= ?��
(3)�ȼҵ�Ǹߺ��ܲ�ҵ�����н�������ȼ�ϵ������ϵĹ��տ��Խ���30�����ϡ�
�ٵ������з�����Ӧ�����ӷ���ʽ��?������������ҺPH?(����䡱�������ߡ����½���)��
�����������SO42-�����ϸߣ����ƹ��������ӱ��Լ���ȥSO42-���ñ��Լ���ѡ�������Լ��е�?��
a��Ba(OH)2 ?b��Ba(NO3)2? c��BaCl2
�ִ������и���ʹ��BaCO3��SO42-����д��������Ӧ�����ӷ���ʽ?��
��ͼ������������Һ����������a��?b��(�>��������=����<��)����ȼ�ϵ���и����Ϸ����ĵ缫��ӦΪ?��
�ο��𰸣���18�֣�
��1��H2O + CO2 =H2 + CO + O2��2�֣�?��ѧ�ܣ�1�֣�
��2��CO �C 2e- +4OH- = CO32- + 2H2O��2�֣�? 2��10-4 mol��L-1��2�֣�
��3����2Cl-+2H2O  ?Cl2��+ H2��+2OH-��2�֣�?���ߣ�1�֣�?
?Cl2��+ H2��+2OH-��2�֣�?���ߣ�1�֣�?
��? ac��2�֣�? BaCO3(s)+ SO42-(aq) = BaSO4 (s)+ CO32-(aq)��2�֣�
��? <��2�֣�? H2-2e-+2OH-=2H2O?��2�֣�
�����������1����ʽ��ӿɵ��ܷ�Ӧ����ʽ��H2O + CO2 =H2 + CO + O2��ͨ���÷�Ӧ��̫����ת��Ϊ�˻�ѧ�ܡ�
��2���ڼ��������£�COʧ����ת��ΪCO32?����ⷽ��ʽΪ��CO �C 2e- +4OH- = CO32- + 2H2O����Һ��pH=12����c(OH?)=0.01mol?L?1��������CO32-�ĵڶ���ˮ�⣬c(HCO3?)=0.01mol?L?1����Kh=c(HCO3?)?c(OH?)/c(CO32?)= 0.01mol?L?1��0.01mol?L?1/0.5mol?L?1= 2��10-4 mol��L-1��
��3���ٵ��ʳ��ˮ����H2��H2��NaOH���������ӷ���ʽΪ��2Cl-+2H2O  ?Cl2��+ H2��+2OH-��������H2O�������H+�õ�������H2��ʹH2O�ĵ���ƽ�������ƶ���OH?Ũ����������pH���ߡ�
?Cl2��+ H2��+2OH-��������H2O�������H+�õ�������H2��ʹH2O�ĵ���ƽ�������ƶ���OH?Ũ����������pH���ߡ�
��Ba(OH)2����SO42?��Ӧ��OH?�ɼ������ȥ��BaCl2����SO42?��Ӧ�����Ҳ����������ʣ�Ba(NO3)2����SO42?��Ӧ����NO3?����ȥ����ac��ȷ��BaCO3ת��Ϊ�����ܵ�BaSO4�����ӷ���ʽΪ��BaCO3(s)+ SO42-(aq) = BaSO4 (s)+ CO32-(aq)��
����ȼ�ϵ���У�����������������ͨ������ļ���������O2�õ�������OH?��ͨ��ȼ�ϵĵ缫�Ǹ���������OH?������a% < b%��������ȼ����������ʧ���ӵ�������Ӧ���缫��ӦʽΪH2-2e-+2OH-=2H2O��
�����Ѷȣ�һ��
4��ѡ���� ��һ�������£����ܱ������з�Ӧ��2NO2(g)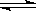 O2(g)+ 2NO(g)����H��0���ﵽ
O2(g)+ 2NO(g)����H��0���ﵽ ƽ�⡣���ı�����һ������X��Y��X�ı仯����ͼ�����ߵ���
ƽ�⡣���ı�����һ������X��Y��X�ı仯����ͼ�����ߵ���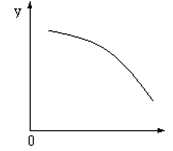
A����X��ʾ�¶�ʱ��Y��ʾNO�����ʵ���
B����X��ʾѹǿʱ��Y��ʾNO2��ת����
C����X��ʾ��Ӧʱ��ʱ��Y��ʾ���������ܶ�
D����X��ʾNO2�����ʵ���ʱ��Y��ʾO2�����ʵ���
�ο��𰸣�B
�����������
�����Ѷȣ�һ��
5��ѡ���� ��10��ʱij��ѧ��Ӧ����Ϊ0.1mol��L-1��s-1�����¶�ÿ����10�淴Ӧ��������Ϊԭ����2����Ϊ�˰ѷ�Ӧ������ߵ�1.6 mol��L-1��s-1����÷�Ӧ����ʲô�¶��½���
[? ]
A.30��
B.40��
C.50��
D.60��
�ο��𰸣�C
���������
�����Ѷȣ�һ��