时间:2025-06-26 02:09:45
1、填空题 (10分)A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有10个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素符号:
A ??, C?,D?,E?
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:??。
(3)写出A、B两元素的最高价氧化 物的水化物之间的相互反应的化学方程式:??。
物的水化物之间的相互反应的化学方程式:??。
(4)比较C、D的最高价氧化物的水化物的酸性:(用化学式表示)
?
参考答案: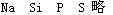
本题解析:略
本题难度:一般
2、填空题 (10分)某非金属单质A经如下图所示的过程转化为含氧酸D,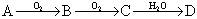 ;已知D为强酸,请回答:
;已知D为强酸,请回答:
(1)若A常温下为 淡黄色固体,B是有刺激性气味的无色气体。
淡黄色固体,B是有刺激性气味的无色气体。
①画出A的原子结构示意图_______________________
②把B通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀化学式为:??
③D的浓溶液在加热的条件下可与Cu反应,该反应的化学方程式为:
?
(2)若A在常温下为气体,C是红棕色气体。
①写出A单质的电子式?。
②C→D的反应中氧化剂与还原剂物质的量之比为:
③写出A与H2反应产物的结构式:?
参考答案:(10分)(1)①?(1分)?② BaSO4(2分)
③Cu+2H2SO4 ==CuSO4+SO2↑+2H2O?(2分)
(2)①略(1分)② 1 :2(2分)③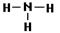 (2分)
(2分)
本题解析:略
本题难度:简单
3、推断题 化合物X的水溶液为浅绿色,可发生如下转化关系(部分反应物、生成物略),其中B、D、E、F均为无色气体,W、K为常见金属单质,C为难溶于水的红褐固体。?在混合液中加入BaCl2溶液可生成不溶于稀盐酸的白色沉淀,H和W反应放出大量的热。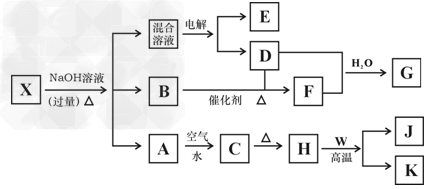
请回答下列问题
(1)B气体的检验方法为_____________
(2)电解混合液时产生D的电极反应为______________?
(3)按要求写出上述转化关系中的有关反应方程式
①含有K元素的化合反应_____________?
②含有K元素的置换反应_____________?
(4)K与过量G的稀溶液反应的离子方程式________________?
(5)物质X的化学式____________,其水溶液的pH_____________7(填大于、小于、等于)。
参考答案:(1)用湿润的红石蕊试纸,变蓝为NH3 ?
(2)4OH--4e-=O2↑+2H2O? ?
(3)①4Fe(OH)2+O2+2H2O=4Fe(OH)3?
②Fe2O3+2Al 2Fe+Al2O3? ?
2Fe+Al2O3? ?
(4)Fe+4H++NO3-=Fe3+ +NO↑+2H2O? ?
(5)(NH4)2Fe(SO4)2?;小于
本题解析:
本题难度:一般
4、填空题 下图是中学化学某些物质之间在一定条件下的相互转化关系,已知A是一种常见的液态化合物,C、D、G、H、K是单质,其它为化合物,G、K是普通钢中的两种重要元素,其中K含量少,E、F对应溶液的酸碱性相反,F的焰色反应为黄色,请按要求作答: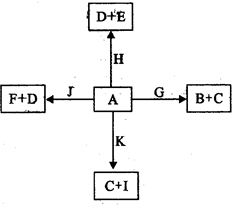
(1)写出化合物的电子式:_________________________。
(2)①写出A与J反应的离子方程式:_______________________________________。
②将少量的H通入F的溶液中,反应的总离子方程式为:_________________________。
(3)B与足量稀硝酸反应,当参加反应的硝酸为4mol,转移电子的物质的量为_________mol(保留2位有效数字)。
(4)已知在200℃,101Kpa下,0.12g单质K与A完全反应生成C与I,吸收了1316J的能量,写出此反应的热化学方程式:_________________________________________。
(5)①以Pt为电极,由I、D以及F的溶液组成原电池,则正极的电极反应为:___________。
②若用此电池电解300mL5mol/L的氯化钠溶液一段时间,两极均收集到标准状况下3.36L气体,此时溶液的pH为_________(假设电解前后溶液体积不变化)。
③若往该电解后所得溶液中通入二氧化碳气体4.48L(标准状况),此时溶液中所有离子浓度的关系由大到小的顺序为:_______________________________________。
参考答案:(1)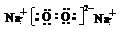 ?
?
(2) ①2H2O+2Na2O2=" 4" Na++4OH-+ O2↑?②2F2+4 OH-= 4F-+ O2+2H2O
(3)0.43
(4)C(s)+H2O(g)=CO(g)+H2(g)?H=+131.6kJ/mol(条件2000C,101Kpa不注明扣一分,状态标错不给分,+漏掉不给分)(2分)?
(5)①O2+4e-+2H2O = 4OH-?(2分)
②14?(2分)?
③c(Na+)>c(Cl-)>c(HCO3―) >c(CO32―)>c(OH-)>c(H+) (2分) (漏写离子不给分)
本题解析:依题意可以推出A+H的反应为2F2+2H2O=4HF+O2,A+G的反应为3Fe+4 H2O=Fe3O4 +4H2, A+K的反应为C+ H2O="CO" + H2.A+J的反应为2Na2O2 +2H2O="4NaOH+" O2,可以完整回答出(1)(2)两问。(3)Fe3O4与HNO3反应时转移的电子数为4*(1/28)*3=0.43mol.(4) C(s)+H2O(g)=CO(g)+H2(g)?H="+131.6kJ/mol(5)" ①O2作正极,O2+4e-+2H2O = 4OH-②2NaCl + 2H2O ="2NaOH" + H2 + Cl2 .通过两极产生气体的体积为3.36L可以算出NaOH的物质的量0.3mol,进而求出NaOH的浓度为1mol/L,pH="14." ③通入4.48L二氧化碳后溶液中有1.2molNaCl,Na2CO3为0.1mol ,NaHCO3为0.1mol。考虑CO32-水解能力大于HCO3-,可以推出各离子的浓度大小关系。
本题难度:困难
5、填空题 化合物X、Y、Z是由短周期的三种元素两两结合而成,X、Y、Z之间的转化关系如右图所示(无被省略的物质):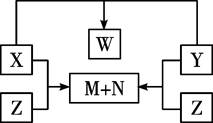
又知:X、N、W均为液态物质,且X与N的组成元素相同。试回答:
(1)上述转化关系图中涉及的基本反应类型是?;
(2)X、Y、Z、W的化学式依次是:
X?、Y?、Z?、W?;
(3)写出X与Y、X与Z反应的化学方程式:
X+Y:?;
X+Z:?。
参考答案:(1)化合反应?(2)H2O2 ?SO2 ?H2S? H2SO4
(3)H2O2+SO2=H2SO4? H2O2+H2S=S↓+2H2O
本题解析:突破口在于X、N、W均为液态物质且X与N的组成元素相同,所以,就初步确定X、N为H2O2和H2O,考虑到H2O2作氧化剂时产物是H2O,可初步认定X为H2O2,N为H2O;Z与H2O2反应,Z应有还原性,联想到H2S、SO2,特别是H2S和SO2可以生成S和H2O,SO2溶于H2O2中可被氧化成H2SO4,所以,整个关系图全部推出。
本题难度:一般