时间:2025-06-26 02:04:51
1、选择题 下列比较中不正确的是
A.酸性HNO3>H3PO4
B.熔点Na<K
C.碱性Ba(OH)2>Sr(OH)2
D.稳定性CH4>SiH4
2、选择题 短周期元素中,原子基态时具有1个未成对电子的元素共有多少种:
A.5
B.6
C.7
D.8
3、简答题 现有A、B、C、D、F六种短周期元素,在化学反应中均能形成简单的阴离子或阳离子,且A、B、C、D离子具有相同的电子层结构.
已知:①常温下,F的单质是一种有色气体,常用于杀菌、消毒;
②A的单质以溶于NaOH溶液,向生成的溶液中通入CO2气体有白色沉淀生成;
③C的氢化物分子G是具有10电子微粒,且以发生下列转化:G
4、选择题 下列各元素中一定属于主族元素的是
[? ]
A.X元素能形成+7价的含氧酸及其盐
B.Y元素的原子最外层有2个电子
C.Z元素的原子最外层电子数等于6
D.R元素的原子次外层有18个电子
5、填空题 看表填空。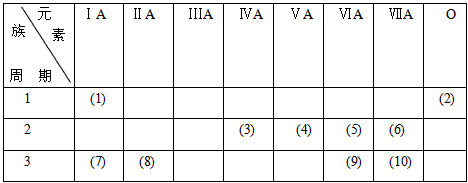
(1)写出(1)-(10)号元素的元素符号:(1)______(2)_____(3)______(4)______(5)______(6)______(7)_______(8)______(9)________(10)______。并指出能成共价键的元素有______种。
(2)(1)、(5)、(9)号元素,相互化合时可形成_______化合物,但溶于水后也可以电离出_______离子和
_______离子。
(3)(8)、(10)号元素化合时,可通过_______键形成_______化合物。
(4)(1)、(5)、(7)号元素相互化合形成的物质中,既有_______键,又有_______键,它的俗称有
_______、_______、_______。
(5)可形成双原子分子的单质有(写化学式):_______、_______、_______、________、_______,原子间以________键结合。
(6)可形成最稳定气态氢化物的元素是________。
(7)(1)、(4)号元素形成的气态氢化物溶于水后,溶液呈_______性,(1)、(10)号元素形成的气态氢化物溶于水后溶液呈_______性。
(8)(3)、(5)、(7)号元素相互化合可形成_______化合物。该物质俗称为_______,但属于_______类物质。
(9)分子中含有18个电子的气态氢化物有____种,分别写出化学式________,将分子中含10个电子的气态氢化物的化学式分别写出:_____、_____、______、_______。
(10)含氧量最高的离子化合物和共价化合物分别是(填化学式)_______和________。
(11)10种元素中化学性质最不活泼的是________。
(12)(3)、(7)、(9)三种元素的最高氧化物的水化物中,碱性由强到弱的顺序是________。