时间:2025-06-26 01:29:38
1、填空题 下列结构图中,代表原子序数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表共价键。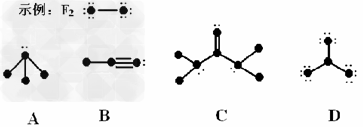
(1)?根据各图表示的结构特点,写出该分子的化学式: A:________?B:_________?C:________?D:________
(2)与D互为等电子体的化学式_______________?
2、选择题 下列分子中所有原子都满足最外层8电子结构的是
[? ]
A.光气(COCl2)
B.六氟化硫
C.二氟化氙
D.三氟化硼
3、选择题 下列有关化学用语正确的是
[? ]
A.次氯酸分子的电子式: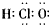
B.丙烯酸的结构简式:CH2CHCOOH
C.质量数为137的钡原子: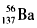
D.Cl-的结构示意图: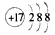
4、填空题 (1)在下列物质中:(A)氩(B)NaOH(C)甲烷(D)氯化钡(E)乙烯(F)NH3(G)CCl4(H)H2O2?①只含离子键的物质是______;②既有离子键又有共价键的化合物是______;③只含极性键的物质是______;④含非极性键的物质是______;(选填序号)
(2)下列变化①碘的升华②烧碱熔化③氯化钠溶于水④氯化氢溶于水⑤氧气溶于水⑥氯化铵受热分解.未发生化学键破坏的是______;仅发生离子键破坏的是______;仅发生共价键破坏的是______.
5、选择题 由短周期的两种元素组成的化合物XY3,下列说法错误的是( )
A.X和Y可能位于同一周期,也可能位于不同周期
B.X可能是金属,也可能是非金属
C.X和Y一定位于不同主族
D.化合物XY3溶于水,溶液可能显碱性