时间:2025-06-26 01:28:06
1、选择题 位于元素周期表第三周期ⅥA族的元素是
[? ]
A.碳
B.氧
C.硫
D.硅
参考答案:C
本题解析:
本题难度:简单
2、选择题 镭是元素周期表中第七周期ⅡA族元素,下列关于镭的叙述中不正确的是
A.镭的金属性比钙的强
B.在化合物中呈+2价
C.其碳酸性盐不溶于水
D.其氢氧化物呈碱性
参考答案:D
本题解析:在周期表中同族金属元素,从上到下其金属逐渐增强,故Ra的金属性应比钙的强;Ra属于第ⅡA族元素,在化合物中应呈+2价;因MgCO3、CaCO3、BaCO3等均难溶于水,可推知Ra的碳酸盐应不溶于水;Ra的氢氧化物的碱性应比Ca(OH)2的更强,而不应呈弱碱性.
本题难度:简单
3、选择题 将O2、CH4、Na2O2放入密闭容器中,在150℃条件下用电火花引燃,充分反应
后,容器中无气体,且将残余物溶于水中无气体放出。则O2、CH4、Na2O2的物质的量之比与反应后容器内固体的成分为?
A. 1:2:6 ;Na2CO3和NaHCO3
B.2:1:4 ;Na2CO3
C. 1:2:6; Na2CO3和NaOH
D. 2:1:4; Na2CO3和NaOH
参考答案:C
本题解析:容器中无气体,且将残余物溶于水中无气体放出,这说明过氧化钠没有剩余,所以根据原子守恒可知,生成物一定是氢氧化钠和碳酸钠,所以反应的化学方程式是O2+2CH4+6Na2O2=2Na2CO3+8NaOH,答案选C。
点评:该题是中等难度的试题,也是高考中的常见题型,难度较大。该题的关键是依据反应现象,借助于原子守恒即可得出正确的结论。该题有利于培养学生的逻辑推理能力和应试能力,提高学生的学习效率。
本题难度:简单
4、选择题 在科技活动晚会上,某同学向甲、乙两张白纸上分别喷洒两种不同的试剂,甲变成一幅蓝色图画,乙变成一幅红色图画,下列叙述不正确的是 (? )
A.甲中的图画事先由淀粉溶液做成,后来喷洒的是碘水
B.乙中的图画事先由NaClO溶液做成,后来喷洒的是酚酞溶液
C.乙中的图画事先由酚酞做成,后来喷洒的是NaOH溶液
D.甲、乙两张纸上均发生了化学反应
参考答案:B
本题解析:略
本题难度:简单
5、填空题 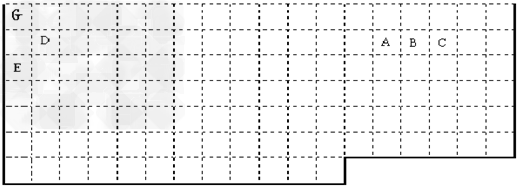
根据信息回答下列问题:
(1) 上表中实线是元素周期表的部分边界,请你用实线标出表的上边界,并把符合下列要求的元素的元素符号标在表中对应位置处。
①?最高价氧化物的水化物碱性最强(放射性元素除外)。?
②?电负性最大。?
③?第一电离能对大。
(2)F元素的原子核外有25个运动状态不同的电子,F元素是__________(名称),F2+的未成对电子数是_____?,与F之具有相同最高正价的另一同周期元素的单质在常温下的状态为___________。(填固态、液态、气态)
(3)列举一种由A、C、E、G四种元素组成的盐____________?。
(4)D的最高价氧化物对应的水化物属两性化合物,证明这一结论的有关离子方程式为_________________、______________。
?(5)元素M基态原子中次外层有5个未成对电子而最外层只有一个电子;?MCl3能与B和C的氢化物共同形成配位数为6的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。MCl3形成的配合物的化学式为________(用具体元素符号表示)。
参考答案:(1)?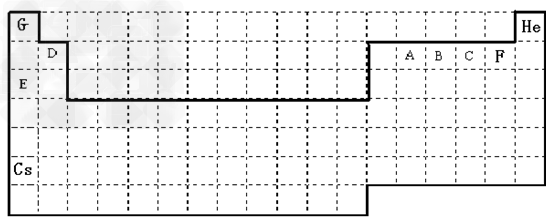
(2)锰?;5?;液态
(3)NaHCO3等有机羧酸的钠盐均可(合理答案均可)
(4)Be(OH)2+2H+===Be2++2H2O?;Be(OH)2+2OH-===BeO22-+2H2O
(5)[Cr(NH3)4(H2O)2]Cl3
本题解析:
本题难度:一般