时间:2025-06-26 01:08:26
1、选择题 下列离子方程式,?正确的是
A.氯化铝溶液与过量氨水 Al3++3NH3・H2O →Al(OH)3↓+3NH4+
B.明矾净水原理:Al3++3H2O →Al(OH)3↓+3H+
C.将足量氯气通入溴化亚铁溶液:2Fe2++Cl2→2Fe3++2Cl-
D.偏铝酸钠溶液与过量盐酸AlO2-+H++H2O →Al(OH)3↓
2、选择题 维生素C具有的性质是:
A.难溶于水
B.强还原性
C.强氧化性
D.加热难分解
3、选择题 下列有机物分子在氢核磁共振谱中只给出一种信号的是
A.HCHO
B.CH3OH
C.HCOOH
D.CH3COOCH3
4、选择题 下列依据相关数据作出的推理和判断中,不正确的是
A.依据溶解度的数据,选择用重结晶的方法可将硝酸钾提纯
B.依据相对分子质量的数据,推测乙醇和丙烷沸点的相对高低
C.依据沸点的数据,判断用分馏的方法从石油中获取汽油和煤油等
D.依据燃烧热的数据、热化学方程式和盖斯定律,可计算一些反应的反应热
5、填空题 化学在环境保护中起着十分重要的作用。催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染。
(1)催化反硝化法中,H2能将NO3-还原为N2。25℃时,反应进行l0 min,溶液的pH由7变为l 2。
①N2的结构式为
②上述反应的离子方程式为 ,其平均反应速率v(NO3-)为 mol・L-1・min-1。
③还原过程中可生成中间产物NO2-,写出2种促进NO2-水解的方法 。
(2)电化学降解NO3-的原理如下图所示。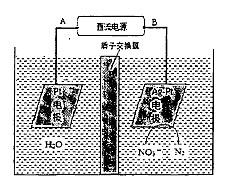
①电源正极为 (填“A”或“B”),阴极反应式为:
②若电解过程中转移了2 mol电子,则膜两侧电解液的质量变化差(△m左-△m右)为 g。