时间:2025-06-26 00:35:42
1、填空题 电石浆是氯碱工业中的一种废弃物,其大致组成如下表所示:
用电石浆可生产无水CaCl2,某化工厂设计了以下工艺流程: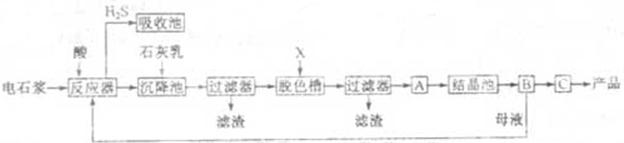
已知氯化钙晶体的化学式是:CaCl2・6H2O;H2S是一种酸性气体,且具有还原性。
(1)反应器中加入的酸应选用 ?①?。
(2)脱色槽中应加入的物质X是?②?;设备A的作用是?③ ;设备B的名称为 ?④?;设备C的作用是 ?⑤?。
(3)为了满足环保要求,需将废气H2S通入吸收池,下列物质中最适合作为吸收剂的是?⑥?。
A.水
B.浓硫酸
C.石灰乳
D.硝酸
(4)将设备B中产生的母液重新引入反应器的目的是?⑦?。
2、选择题 粗碘中通常含ICl和IBr,称为卤素互化物,其性质和卤素单质相似,都是较强的氧化剂,而且受热时ICl和IBr皆可像I2一样升华,在粗碘中加入以下选项中的一种物质后,再进行升华可制得精碘,应加入的物质是( )。
A.H2O
B.Zn
C.KI
D.KCl
3、选择题 下列关于海洋资源开发和利用的叙述, 不正确的是
A.海水经过风吹日晒,逐渐蒸发,可制得食盐等物质
B.海水蕴藏着丰富的化学资源
C.地球表面大部分被海水覆盖,故人类不存在缺水问题
D.开发海洋资源应遵循可持续发展的原则
4、选择题 将过量的CO2分别通入①CaCl2溶液,②Na2SiO3溶液,③Ca(ClO)2溶液,④饱和Na2CO3溶液,最终有沉淀析出的是( )
A.①②③④
B.②④
C.①②③
D.②③
5、选择题 下列说法正确的是( )
A.制取水泥和玻璃的原料中均有纯碱
B.普通玻璃是电的绝缘体,这种透明的固体物质是混合物,并有固定的熔点
C.等物质的量的?SiO2与CaCO3在高温下锻烧,残留物为一纯净物
D.水泥具有水硬性,在空气中能硬化,但在水中不能硬化