时间:2025-06-26 00:34:57
1、推断题 下列中学化学中常见物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其他为化合物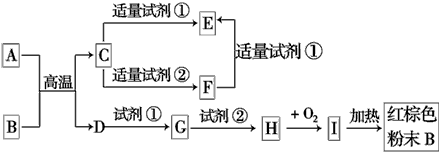
试推断:
(1)写出物质的化学式:A:____________、C:____________、I:____________。
(2)写出下列反应的方程式: C→F的离子方程式_____________________________。 H→I的化学方程式_______________________。
参考答案:(1)Al;Al2O3;Fe(OH)3
(2)Al2O3+2OH-==2AlO2-+H2O;4Fe(OH)2+O2+2H2O==4Fe(OH)3
本题解析:
本题难度:一般
2、推断题 下图每一方框中的字母代表一种反应物或生成物。产物J是含金属元素A的白色胶状沉淀,I为NaCl溶液,D是淡黄色固体。试填写下列空白: 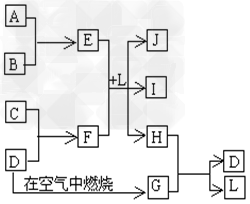
(1)框图中所列物质中属于非电解质的物质名称为?___________;
(2)用电子式表示出H的形成过程__________________;
(3)将E的水溶液蒸干并灼烧得到的固体物质的化学式为_______________; ?
(4)F的水溶液中各离子浓度由大到小的顺序为_________________?;
(5)F的水溶液显碱性的原因:(用离子方程式表示)?_________________;
(6)E与F在L中反应的离子方程式为____________________;
(7)H和G之间反应的化学方程式为____________________。
参考答案:(1)二氧化硫?
(2)“略”?
(3)Al2O3
(4)c(Na+)>c(S2-)>c(OH-)>C(HS-)>c(H+)?
(5)S2-+H2O HS-+OH-?
HS-+OH-?
(6)3Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑?
(7)2H2S+SO2=3S↓+H2O
本题解析:
本题难度:一般
3、选择题 X、Y、Z是三种常见元素的单质,甲、乙是两种常见的化合物,这些单质和化合物之间存在如图所示的转化关系,下列说法正确的是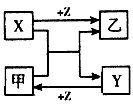
[? ]
A.X、Y、Z一定是非金属单质
B.X、Y、Z中至少有一种是金属单质
C.若X、Y都为金属单质,则Z必为非金属单质
D.若甲为FeI2,则乙可能为FeCl2
参考答案:C
本题解析:
本题难度:一般
4、简答题 A-M分别代表一种物质.其中,A、D、I、M的焰色反应呈紫色(透过蓝色钴玻璃),实验室常用I在MnO2催化作用下加热制备氧气;B、C是短周期元素组成的气体单质,且C为黄绿色;E是短周期元素组成的常见金属单质,它既能与D溶液反应,也能与G溶液反应.
请回答下列问题:
(1)组成E的元素位于周期表中第______周期,______族.
(2)C与H反应得到的含氧酸的电子式为______.
(3)E与D溶液反应的离子方程式是______.
(4)向M溶液中逐滴加入G溶液至过量的现象是______.
(5)在加热条件下K与碳酸钾反应的化学方程式是______.
(6)在足量的稀硫酸中,I与A以物质的量之比1:1反应,可以得到一种高效消毒剂ClO2及其他产物,该反应的化学方程式是______.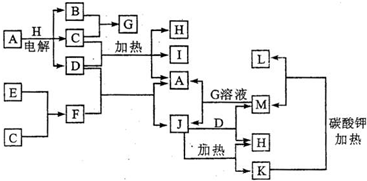
参考答案:A、D、I、M的焰色反应呈紫色(透过蓝色钴玻璃),都含有K元素,实验室常用I在MnO2催化作用下加热制备氧气,I为KClO3,B、C是短周期元素组成的气体单质,且C为黄绿色,C为Cl2;
A+H电解
本题解析:
本题难度:一般
5、简答题 中学化学中常见的物质有如图所示的转化关系(反应条件略去).X、Y、Z、W是单质,其余均为化合物,A、W、Z常温下呈气态,且A是一种大气污染物,B是一种常用的酸.
(1)写出下列物质的化学式:
Y______、A______、C______.
(2)D的电子式为______.
(3)我国生产B的工业中,常采用以下方式处理尾气A: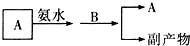
试从综合经济效益的角度分析,这样处理的目的是(答出其中两点即可):
a.______;b.______.
(4)反应①的化学方程式:______.
反应②的化学方程式:______.
反应④的离子方程式:______.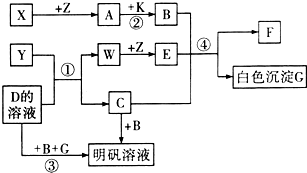
参考答案:A是一种大气污染物,可能为SO2或NO2,由题目可知,X、Z中只有Z为气体,则X应为S,Z为O2,A为SO2,B是一种常用的酸,应为H2SO4,题中SO2和K反应生成H2SO4,则K应为氧化性物质H2O2,H2SO4和C反应生成明矾,则C应为KAlO2,所以Y和D应为Al和KOH溶液的反应,则Y为Al,D为KOH,W为H2,E为H2O,生成物G为Al(OH)3,F为K2SO4,则
(1)由以上分析可知,Y为Al,A为SO2,C为KAlO2,故答案为:Al、SO2、KAlO2;
(2)D为KOH,为离子化合物,电子式为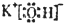
,故答案为: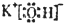
;
(3)二氧化硫和氨水反应生成亚硫酸铵,进而与过氧化氢反应生成硫酸铵,可减少SO2对环境污染、使原料利用率得到提高、副产品可作化肥,
故答案为:a.减少SO2对环境污染;b.可以使原料利用率得到提高;c.副产品可作化肥,社会需求量大(任意填两种)
(4)反应①Al和KOH溶液的反应,反应的化学方程式为2Al+2KOH+2H2O=2KAlO2+3H2↑,反应②为H2O2和SO2的反应,反应的化学方程式为H2O2+SO2=H2SO4,反应④KAlO2与酸的反应,生成Al(OH)3沉淀,反应的离子方程式为AlO2-+H++H2O=Al(OH)3,
故答案为:2Al+2KOH+2H2O=2KAlO2+3H2↑;H2O2+SO2=H2SO4;AlO2-+H++H2O=Al(OH)3↓.
本题解析:
本题难度:一般