时间:2025-06-26 00:15:20
1、填空题 科学家从化肥厂生产的(NH4)2SO4中检出组成N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以
SO42-和N4H44+两种离子形式存在,植物的根系极易吸收N4H44+,但它遇到碱时,会生成一种类似白磷的N4分子,N4分子不能被植物吸收。请回答下列问题:
(1)N4和N2的关系正确的是___________(填序号);
A.同种单质 B.同位素 C.同分异构体 D.同素异形体
(2)N4H4(SO4)2______ (填“能”或“不能”)和草木灰混合施用;
(3)已知白磷、NH4+、N4H44+的空间构型均为四面体,NH4+的结构式为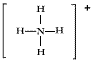 (→表示共用电子对由N原子单方面提供),白磷(P4)的结构式为
(→表示共用电子对由N原子单方面提供),白磷(P4)的结构式为 。请画出N4H44+的结构式__________________。
。请画出N4H44+的结构式__________________。
(4)已知液氨中存在着平衡2NH3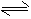 NH4++NH2-。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:______________________
NH4++NH2-。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:______________________
2、选择题 臭氧分子的结构如图,呈V型,三个原子以一个O原子为中心,与另外两个O原子分别构成共价键;中间O原子提供2个电子,旁边两个O原子各提供一个电子,构成一个特殊的化学键:三个O原子均等地享用这4个电子。则下列微粒中与O3的结构最相似的是 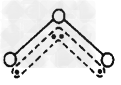
[? ]
A.SO2?
B.C3H6?
C.CO2?
D.CNO-
3、选择题 按下列四种有关性质的叙述,可能属于金属晶体的是(? )
A.由分子间作用力结合而成,熔点很低
B.固体或熔融后易导电,熔点在1000 ℃左右
C.由共价键结合成网状晶体,熔点很高
D.固体不导电,但溶于水或熔融后能导电
4、选择题 已知X、Y、Z二种元素组成的化合物是离子晶体,其晶胞如图l所示,则下列表示该化合物的化学式正确的是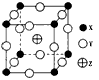
[? ]
A.ZXY3
B.ZX2Y6
C.ZX4Y8
D.ZX8Y12
5、选择题 下列晶体中,熔点最高的是(?)
A.KF
B.MgO
C.CaO
D.NaCl