时间:2025-06-26 00:11:15
1、选择题 精确配制一定物质的量浓度的NaOH溶液,下面实验操作中,正确的是( )
A.将烧杯中已冷却的NaOH溶液转移到未经干燥的容量瓶中
B.将称好的NaOH固体放入容量瓶中,加入少量水溶解
C.在烧杯中溶解NaOH固体后,立即将所得溶液注入容量瓶中
D.称量时,将NaOH固体直接放在天平托盘上面的纸上
参考答案:A
本题解析:
本题难度:简单
2、填空题 (1)写出下图中序号①~③仪器的名称:
①______;②______;③______.
(2)仪器①~④中,使用时必须检查是否漏水的有______.(填仪器序号)
(3)如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容.现用该浓硫酸配制480mL1mol?L-1的稀硫酸.
可供选用的仪器有:
①胶头滴管②烧瓶③烧杯④玻璃棒⑤药匙⑥量筒⑦托盘天平. 请回答下列问题:
请回答下列问题:
a.该硫酸的物质的量浓度为______mol?L-1.
b.配制稀硫酸时,还缺少的仪器有______(写仪器名称).
c.经计算,配制480mL1mol?L-1的稀硫酸需要用量筒量取上述浓硫酸的体积为______mL.
d.对所配制的稀硫酸进行测定,发现其浓度大于1mol?L-1,配制过程中下列各项操作可能引起该误差的原因有______.
A.定容时,俯视容量瓶刻度线进行定容.
B.将稀释后的稀硫酸立即转入容量瓶后,紧接着就进行以后的实验操作.
C.转移溶液时,不慎有少量溶液洒到容量瓶外面.
D.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水.
E.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处.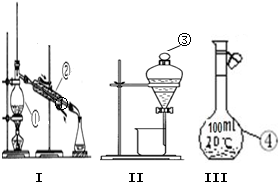
参考答案:(1)①根据①的构造可知,①为蒸馏操作中的主要仪器:蒸馏烧瓶,
故答案为:蒸馏烧瓶;
②仪器②为蒸馏操作中冷凝流出物的仪器:冷凝管,
故答案为:冷凝管;
③仪器③为分离互不相溶液体的仪器:分液漏斗,
故答案为:分液漏斗;
(2)①为蒸馏烧瓶、②为冷凝管、③为分液漏斗、④为容量瓶,其中①和②在使用前必须要检查是否漏水,而①分液漏斗有旋塞,使用前必须检查是否漏水,避免旋塞漏水,影响分离效果,③容量瓶在使用前也需要检查是否漏水,避免摇匀操作时漏液,
故答案为:③④;
(3)a.该浓硫酸的物质的量浓度为:1000×1.84×98%98mol/L=18.4mol/L,故答案为:18.4;
b.配制一定物质的量浓度的溶液步骤为:计算、量取、稀释、冷却、转移、洗涤、定容、摇匀等,需要选用的仪器为:量筒、烧杯、玻璃棒、容量瓶、胶头滴管、500mL容量瓶等,还缺少500mL容量瓶,
故答案为:500ml容量瓶;
c.配制480mL1mol?L-1的稀硫酸,实际上配制的是500mL 1mol/L的稀硫酸,配制500mL 1mol/L的稀硫酸,需要量取的浓硫酸的体积为:1mol/L×0.5L18.4mol/L≈0.0272L=27.2mL,
故答案为:27.2;
d.A.定容时,俯视容量瓶刻度线进行定容,会导致加入的蒸馏水体积偏小,配制的溶液浓度偏高,故A正确;
B.将稀释后的稀硫酸立即转入容量瓶后,紧接着就进行以后的实验操作,热的溶液体积偏大,冷却后溶液体积变小,配制的溶液浓度偏高,故B正确;
C.转移溶液时,不慎有少量溶液洒到容量瓶外面,导致配制的溶液中溶质的物质的量偏小,配制的溶液浓度偏低,故C错误;
D.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水,对溶质的物质的量和溶液体积没有影响,不影响配制结果,故D错误;
E.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处,导致配制的溶液体积偏大,配制的溶液浓度偏低,故E错误;
故答案为:AB.
本题解析:
本题难度:一般
3、填空题 今欲用NaHCO3固体配制480mL?0.2mol/L的NaHCO3溶液.根据题意填空:
(1)配制该溶液应选用______?mL容量瓶.
(2)用托盘天平称取______?g固体NaHCO3.
(3)将称好的NaHCO3固体放至500mL的大烧杯中,倒入约250mL蒸馏水,用玻璃棒搅拌至完全溶解.待冷却至室温后,将烧杯中的溶液用玻璃棒引流转移至容量瓶.
(4)用少量蒸馏水洗涤烧杯2-3次,并将每次洗涤的溶液都注入容量瓶,轻轻晃动容量瓶,使溶液混和均匀.
(5)向容量瓶中加入蒸馏水,直到液面离刻度线约2-3厘米时,改用______?滴加蒸馏水至液面与刻度线相切.盖好瓶塞,摇匀.
(6)配制好的溶液______(填“能”或“不能”)长期存放在容量瓶中.
(7)以下因素会造成实验结果偏低的是______
A.定容时观察液面仰视? B.定容时观察液面俯视
C.有少量NaOH溶液残留在烧杯中? D.容量瓶中原来有少量蒸馏水.
参考答案:(1)配制?0.2mol/L的NaHCO3溶液480mL,没有480mL的容量瓶,选择大于480mL,且体积相近的容量瓶.故应选择500mL容量瓶.
故答案为:500.
(2)需碳酸氢钠的质量为m=0.5L×0.2mol?L-1×84g/mol=8.4g.
故答案为:8.4.
(5)操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,盖好瓶塞,摇匀.
故答案为:胶头滴管.
(6)容量瓶不能长期盛放液体,配好的溶液应转移到试剂瓶中,贴标签存放.
故答案为:不能.
(7)A.定容时观察液面仰视,使溶液的体积偏大,所以溶液浓度偏低;
B.定容时观察液面俯视,使溶液的体积偏低,所以溶液浓度偏高;
C.有少量NaOH溶液残留在烧杯中,转移到容量瓶中氢氧化钠的质量减小,溶液浓度偏低;
D.最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响.
故选:AC
本题解析:
本题难度:一般
4、选择题 用1g NaOH固体配制成0.5mol/L NaOH溶液,所得溶液的体积是
[? ]
A.0.5ml
B.5ml
C.50ml
D.500ml
参考答案:C
本题解析:
本题难度:简单
5、选择题 用NaOH固体配制1mol/L的NaOH溶液,下列操作和说法中正确的是( )
A.将40?g?NaOH固体溶于1L水中可配成1?mol/L的NaOH溶液
B.称量时,将固体NaOH直接放在天平右盘上
C.固体溶解后冷却到室温,然后将溶解后溶液转移到容量瓶中,立即向容量瓶中直接加水稀释到刻度线
D.配制溶液时容量瓶中原来有少量蒸馏水不会影响实验结果
参考答案:A、40gNaOH的物质的量为1mol,溶于水配成1L溶液,所得溶液的浓度为1mol/L,体积1L是指溶液的体积,不是溶剂的体积,故A错误;
B、氢氧化钠具有腐蚀性且易潮解,应将氢氧化钠放在烧杯中,将盛有氢氧化钠的烧杯放在天平左盘进行迅速称量,故B错误;
C、烧杯壁、玻璃棒上沾有少量氢氧化钠,若不洗涤,移入容量瓶内的氢氧化钠的质量减少,所配溶液的浓度偏低,故C错误;
D、溶液配制需加水定容,容量瓶中有少量蒸馏水对所配溶液无影响,故D正确;
故选D.
本题解析:
本题难度:简单