ʱ��:2025-06-25 23:36:56
1��ѡ���� �ڵ��ˮ��ȡH2��O2ʱ��Ϊ����ǿ�����ԣ�����Ҫ����һЩ����ʣ����ѡ��
[? ]
A��NaOH
B��HCl
C��NaCl
D��CuSO4
�ο��𰸣�A
���������
�����Ѷȣ�һ��
2������� ��16�֣�ij��ѧ��ȤС���̼������������������о���ȡ����һЩ�ɹ���
��֪��C(s)+O2(g)  CO2(g) ��H=-393kJ?mol-1��
CO2(g) ��H=-393kJ?mol-1��
2CO (g)+O2(g)  2CO2(g) ��H=-566kJ?mol-1��
2CO2(g) ��H=-566kJ?mol-1��
2H2(g)+O2(g)=2H2O(g) ��H=-484kJ?mol-1
��1����ˮ�����絽���ȵ�̿��ʵ��̿���������Ƶ�CO��H2�����÷�Ӧ���Ȼ�ѧ����ʽΪ ��
��2��)��һ����CO(g)��H2O(g)�ֱ�ͨ���ݻ�Ϊ1L�ĺ����ܱ������У�������Ӧ��
CO(g)+H2O(g) CO2(g)+H2(g)���õ������������ݣ�
CO2(g)+H2(g)���õ������������ݣ�
| ʵ������ | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | |
| H2O | CO | CO2 | |||
| 1 | 500 | 4 | 8 | 3.2 | 4 |
| 2 | 750 | 2 | 4 | 0.8 | 3 |
| 3 | 750 | 2 | 4 | 0.8 | 1 |

 2CO+O2��������Ϊ��Һ�е�OH-�ŵ磬�������ĵ缫��ӦʽΪ ��
2CO+O2��������Ϊ��Һ�е�OH-�ŵ磬�������ĵ缫��ӦʽΪ ���ο��𰸣���1����2�֣�C(s)+H2O(g)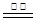 CO(g)+H2(g) ��H=+132kJ?mol-1
CO(g)+H2(g) ��H=+132kJ?mol-1
��2���ٷ���(2��) ��0.8mol/(L��min) (2��)
��20%((2��) �ܼӴ���(2��) [��������ͼ] 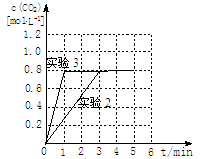 ��2�֣�
��2�֣�
��3����2�֣�4OH--4e-=O2��+2H2O
��4����2�֣�CO+2Ag(NH3)2OH=2Ag��+(NH4)2CO3+2NH3
�����������1����֪����C(s)+O2(g)  CO2(g) ��H=-393kJ?mol-1����2CO (g)+O2(g)
CO2(g) ��H=-393kJ?mol-1����2CO (g)+O2(g)  2CO2(g) ��H=-566kJ?mol-1����2H2(g)+O2(g)=2H2O(g) ��H=-484kJ?mol-1�����ݸ�˹���ɣ��١��ڡ�1/2���ۡ�1/2�ø÷�Ӧ���Ȼ�ѧ����ʽΪC(s)+H2O(g)
2CO2(g) ��H=-566kJ?mol-1����2H2(g)+O2(g)=2H2O(g) ��H=-484kJ?mol-1�����ݸ�˹���ɣ��١��ڡ�1/2���ۡ�1/2�ø÷�Ӧ���Ȼ�ѧ����ʽΪC(s)+H2O(g)  CO(g)+H2(g) ��H=+132kJ?mol-1����2���ٸ��������Ӧ�͵�Чƽ��֪ʶ֪���¶�Ϊ500��ʱ����ʼ�����м���2molH2O��4molCOʱ����ƽ���CO2�����ʵ���Ϊ1.6mol��750��ʱ��ƽ���CO2�����ʵ���Ϊ0.8mol���������¶ȣ�ƽ�������ƶ����÷�Ӧ������ӦΪ���ȷ�Ӧ���ڸ��������Ӧ֪��v(H2)= v(CO2)��ʵ��1�У�0��4minʱ���ڣ�v(H2)=3.2�£�1��4��="0.8" mol/(L��min)���۷����������֪��ʵ��2�ﵽƽ��ʱCO��ת����=0.8/4��100%=20%����ʵ��3��ʵ��2��ȣ���ѧƽ��û���ƶ���ֻ�������˴�ƽ��ʱ�䣬����������㶨Ϊ1L���ʸı�������ǼӴ�����ͼ����𰸣���3����������������Ϊ��Һ�е�OH-�ŵ磬�������ĵ缫��ӦʽΪ4OH--4e-=O2��+2H2O����4����COͨ��������Һ�п�������ɫ�Ľ������������䷴Ӧ����ʽΪCO+2Ag(NH3)2OH=2Ag��+(NH4)2CO3+2NH3��
CO(g)+H2(g) ��H=+132kJ?mol-1����2���ٸ��������Ӧ�͵�Чƽ��֪ʶ֪���¶�Ϊ500��ʱ����ʼ�����м���2molH2O��4molCOʱ����ƽ���CO2�����ʵ���Ϊ1.6mol��750��ʱ��ƽ���CO2�����ʵ���Ϊ0.8mol���������¶ȣ�ƽ�������ƶ����÷�Ӧ������ӦΪ���ȷ�Ӧ���ڸ��������Ӧ֪��v(H2)= v(CO2)��ʵ��1�У�0��4minʱ���ڣ�v(H2)=3.2�£�1��4��="0.8" mol/(L��min)���۷����������֪��ʵ��2�ﵽƽ��ʱCO��ת����=0.8/4��100%=20%����ʵ��3��ʵ��2��ȣ���ѧƽ��û���ƶ���ֻ�������˴�ƽ��ʱ�䣬����������㶨Ϊ1L���ʸı�������ǼӴ�����ͼ����𰸣���3����������������Ϊ��Һ�е�OH-�ŵ磬�������ĵ缫��ӦʽΪ4OH--4e-=O2��+2H2O����4����COͨ��������Һ�п�������ɫ�Ľ������������䷴Ӧ����ʽΪCO+2Ag(NH3)2OH=2Ag��+(NH4)2CO3+2NH3��
���㣺�����Ȼ�ѧ����ʽ��д����˹���ɣ���ѧ��Ӧ���ʺͻ�ѧƽ�⣬�缫��Ӧʽ����ѧ����ʽ����д��
�����Ѷȣ�����
3������� ��ͼ��ʾװ���У��ס��ҡ��������ձ����ηֱ�ʢ��100g5.00%��NaOH��Һ��������CuSO4��Һ��100g
10.00%��K2SO4��Һ���缫��Ϊʯī�缫�� 
��1����ͨ��Դ������һ��ʱ���ñ���K2SO4Ũ��Ϊ10.47%������c�缫�������ӡ�
�ݴ˻ش����⣺
�� ��Դ��N��Ϊ___________����
�� �缫b�Ϸ����ĵ缫��ӦΪ___________��
�� ��ʽ����缫b�����ɵ������ڱ�״���µ������___________��
�� �缫c�������仯��___________g��
�� ���ǰ�����Һ���ᡢ���Դ�С�Ƿ����仯��������ԭ��
����Һ____________________������Һ___________________������Һ______________________��
��2�������������ͭȫ����������ʱ����ܷ�������У�Ϊʲô��____________________________________________��
�ο��𰸣���1������������4OH--4e-==2H2O+O2������2.8L����16g���ݼ�������Ϊ�൱�ڵ��ˮ���Ҽ�С��OH-
�ŵ磬H+���ࣻ�����䣬�൱�ڵ��ˮ
��2�����ԣ���ΪCuSO4��Һ��ת��ΪH2SO4��Һ����ӦҲ�ͱ�Ϊˮ�ĵ�ⷴӦ
���������
�����Ѷȣ�һ��
4��ѡ���� �ö��Ե缫���NaCl��CuSO4���Һ250 mL,����һ��ʱ���,�������õ�11.2 L����(��״����),�������й�������,��ȷ���ǣ�?��
A�����������ķ�Ӧֻ��:4OH--4e-=2H2O+O2��
B�������õ��������Ϊ�������
C����Cu2+��ʼŨ��Ϊ1 mol��L-1,��c(Cl-)��ʼΪ 2 mol��L-1
D��Cu2+����ʼ���ʵ���Ӧ����0.5 mol
�ο��𰸣�C
�������������һ��ʼ��Cl-�ŵ�,Ȼ��OH-�ŵ�,A��;���ݷŵ�˳��,������,һ��ʼCu2+�ŵ�,����������,����ֻ��H+�ŵ����0.5 mol H2,B��;��Cu2+��ʼŨ��Ϊ1 mol��L-1,��������ͨ��1.5 mol e-,��������11.2 L����(��״����),ת��1.5 mol e-,�����������ʵ���Ϊx,���������ʵ���Ϊy,��x+y="0.5" mol,2x+4y="1.5" mol,���,x="y=0.25" mol,C��;���ݼ���˼ά,������������0.5 mol����ȫ��������ת��2 mol e-,������������,��ת�Ƶĵ���С��2 mol,��������������ת�Ƶ���1 mol,�ʲ���ͭ�Ĺ�����ת�Ƶ���С��1 mol,��Cu2+����ʼ���ʵ���ӦС��0.5 mol,D����
�����Ѷȣ�һ��
5��ѡ���� ��25��ʱ���ò��缫���һ������Na2SO4������Һ��һ��ʱ�����������amol���壬ͬʱ��Һ������bg Na2SO4��10H2O���������һ�������¶Ȳ��䣬���ʱNa2SO4��Һ�����ʵ���������Ϊ��?��
A����71/161����100�G
B����71b/161(18a+b)����100�G
C����b/(18a+b)����100�G
D����71b/161(36a+b)����100�G
�ο��𰸣�B
�����������
�����Ѷȣ���