时间:2025-06-25 23:18:06
1、选择题 海水的综合利用可以制备金属钠和镁,其流程如下图所示:
下列说法不正确的是(?)
A.要检验母液中是否含氯离子应当用硝酸酸化的硝酸银溶液进行实验
B.上述流程中所有反应都是非氧化还原反应
C.上述流程中生成Mg(OH)2沉淀的离子方程式为:Mg2++Ca(OH)2= Mg(OH)2+Ca2+
D.不用电解MgO来制取镁是因为MgO熔点高,能耗大
参考答案:B
本题解析:母液中加入石灰乳生成氢氧化镁,离子方程式为Mg2++Ca(OH)2= Mg(OH)2+Ca2+,C正确;检验母液中Cl-用硝酸银溶液和稀硝酸,A正确;上述流程中氯化镁电解生成镁和氯气是氧化还原反应,B错误;工业上电解氯化镁制镁而不是电解氧化镁制镁,因氧化镁熔点高,D正确。
点评:石灰乳是氢氧化钙的悬浊液,书写离子方程式时不能拆开;石灰水是氢氧化钙水溶液,书写离子方程式时,需拆开。
本题难度:一般
2、填空题 (14分) 草酸亚铁用作分析试剂及显影剂等,其制备流程如下: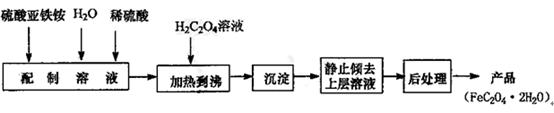
⑴配制(NH4)2Fe(SO4)2 6H2O溶液时,需加少量稀硫酸,目的是?。
6H2O溶液时,需加少量稀硫酸,目的是?。
⑵将制得的产品在氩气气氛中进行热重分析,结果如右图(TG%表示残留固体质量占原样品总质量的百分数)。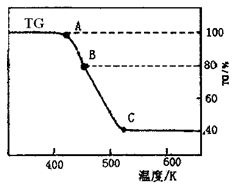
①则C处时残留物的化学式为??。
②有研究学者在实验过程中用气相色谱还检出H2,最终产物中也有微量的磁性物质生成,请你猜想用一个方程式解释这种事实:??。
③现取在真空中146℃脱水后的FeC2O41.44g放在某真空的密闭容器中,再充入0.04molCO。加热至1100℃,其中FeO(s)+CO(g)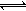 Fe(s)+CO2(g)反应平衡常数K=0.4,则该反应达平衡时,FeO的转化率为多少???。
Fe(s)+CO2(g)反应平衡常数K=0.4,则该反应达平衡时,FeO的转化率为多少???。
(3)金属镁在国民生产中有重要作用,常以MgCl2为原料获取,温度和压强P(HCl)g对MgCl2・6H2O晶体热分解产物的影响如图所示。结合右图请回答下列问题: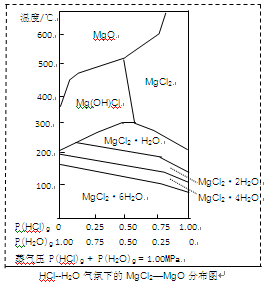
①写出P(HCl)g = 0.25MPa,温度从300℃升高到550℃时反应的化学方程式?;
②实际生产中,将MgCl2・6H2O晶体加热到600℃的过程中几乎得不到无水MgCl2,其原因是?;若要得到无水MgCl2须采取的措施是??。
参考答案:⑴抑制Fe2+水解?⑵①FeO
②3FeO(s)+H2O(g) Fe3O4(s)+H2(g)?③71.4%
Fe3O4(s)+H2(g)?③71.4%
(3)①Mg(OH)Cl ="=" MgO + HCl↑?
②P(HCl)小,加热时Mg2+会发生水解,主要产物是MgO?
通入HCl气体,增大P(HCl),保证其分压大于0.75,抑制Mg2+水解。
本题解析:(1)氩铁离子在水中会发生水解而使溶液显酸性,所以加入稀硫酸可防止水解。氩气性质稳定,常用作保护气,由图像可知在C处剩余固体的质量不再发生变化,所以最终的固体是FeO。磁性物质有关是Fe3O4,又因为还有氢气生成,所以方程式为3FeO(s)+H2O(g) Fe3O4(s)+H2(g)。FeC2O4在真空中分解的方程式为FeC2O4→FeO+CO↑+CO2↑,即1.44g可生成氧化亚铁、CO2、CO各是0.01mol。
Fe3O4(s)+H2(g)。FeC2O4在真空中分解的方程式为FeC2O4→FeO+CO↑+CO2↑,即1.44g可生成氧化亚铁、CO2、CO各是0.01mol。
FeO(s)+CO(g)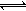 Fe(s)+CO2(g)
Fe(s)+CO2(g)
起始量(mol)? 0.01? 0.05? 0? 0.01
转化量(mol)? x? x? x? x
平衡量(mol)? 0.01-x? 0.05-x? x? x+0.01
根据平衡常数的表达式可知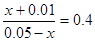 ,解得x=0.00714,所以其转化率是71.4%。
,解得x=0.00714,所以其转化率是71.4%。
(2)由图像可知在是300℃时Mg(OH)Cl,当加热到550℃时,生成物是氧化镁和氯化氢,所以方程式为Mg(OH)Cl ="=" MgO + HCl↑。在常压下镁离子易水解生成氢氧化镁,灼烧即得到氧化镁。要得到无水MgCl2须防止水解,所以要通入氯化氢气体且要压强大于0.75Mpa。
本题难度:一般
3、选择题 下列说法正确的是
A.蛋白质、纤维、蔗糖、聚乙烯、淀粉都是高分子化合物
B.研制乙醇汽油(汽油中添加一定比例的乙醇)技术,可以降低机动车辆尾气中有害气体排放
C.使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用
D.石油、煤、天然气、可燃冰、植物油都属于化石燃料
参考答案:B
本题解析:A.蔗糖不是高分子化合物,排除
B.正确
C.太阳能热水器是将太阳能直接转换为热能,不涉及到生物质能的利用,排除
D.植物油不属于化石燃料
故答案为B
本题难度:一般
4、填空题 (10分)综合利用海水可以制备食盐、纯碱、金属镁、溴等物质,其流程如下图所示: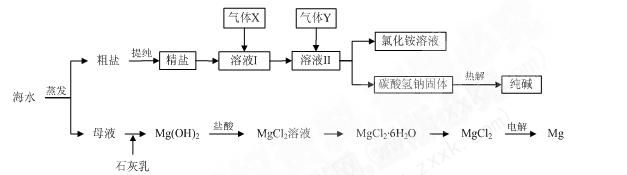 ?
?
(1)粗盐中含有硫酸钠、氯化镁、氯化钙等可溶性杂质,为除去这些杂质而得精盐,进行如下操作:①溶解;②加过量的BaCl2溶液;③加过量的NaOH溶液;④加过量的Na2CO 3溶液;⑤? ▲?;⑥加适量的盐酸;⑦? ▲?。
3溶液;⑤? ▲?;⑥加适量的盐酸;⑦? ▲?。
(2)溶液Ⅱ中发生反应的化学方程式是:? ▲?。
(3)Mg(OH)2沉淀中因混有Ca(OH)2,可选用? ▲?溶液进行洗涤以除之。
(4)高温灼烧六水 合氯化镁晶体(MgCl2・6H2O)所得固体是氧化镁,试写出该反应的化学方程式? ▲?。
合氯化镁晶体(MgCl2・6H2O)所得固体是氧化镁,试写出该反应的化学方程式? ▲?。
(5)若在母液中通入氯气可提取海水中的溴,反应的离子方程式为:? ▲?。
参考答案:
本题解析:略
本题难度:一般
5、选择题 下列不属于水泥的成分的是( )
A.2CaO?SiO2
B.3CaO?SiO2
C.2Na2O?SiO2
D.3CaO?Al2O3
参考答案:C
本题解析:
本题难度:简单