时间:2025-06-25 22:38:04
1、简答题 甲同学设计如图所示装置研究氯气能否与水发生反应.气体a的主要成分是含有少量空气和水蒸气的氯气.
请回答下列问题:
(1)浓硫酸的作用是______.
(2)证明氯气和水反应的实验现象为______.
(3)从物质性质的方面来看,这样的实验设计存在的缺陷为______,请用离子方程式表达图中D框克服事故隐患的措施______.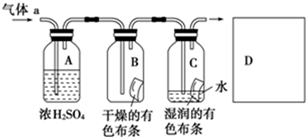
参考答案:(1)浓硫酸具有吸水性,常用作干燥剂,在实验中吸收气体a中的水蒸气,
故答案为:除去氯气中的水蒸气,干燥氯气;
(2)干燥氯气不具有漂白性,氯气和水反应生成盐酸和次氯酸,方程式为:Cl2+H2O=HCl+HClO,次氯酸具有漂白性,
故答案为:装置B中的有色布条不褪色,装置C中的有色布条褪色;
(3)氯气有毒,应进行尾气处理,不能随意排放到空气中,可用碱溶液来吸收:Cl2+2NaOH=NaCl+NaClO+H2O,离子方程式为:Cl2+2OH-=Cl-+ClO-+H20;
故答案为:没有尾气吸收装置;Cl2+2OH-=Cl-+ClO-+H20.
本题解析:
本题难度:简单
2、选择题 下列关于氯气的物理性质描述正确的是( )
A.无毒
B.无颜色
C.无气味
D.有刺激性气味
参考答案:氯气是一种黄绿色、有剧烈刺激性气味,密度比空气大,能溶于水,有毒的气体.
A.氯气人吸入少量,会使鼻和喉头的粘膜受到刺激,引起胸部疼痛和咳嗽,吸人大量会中毒死亡,氯气是有毒的气体,故A错误;
B.氯气是一种黄绿色的气体,故B错误;
C.氯气是有剧烈刺激性气味的气体,故C错误;
D.氯气是有剧烈刺激性气味的气体,故D正确;
故选D.
本题解析:
本题难度:简单
3、选择题 下列物质中同时含有氯分子和氯离子的是
液氯? B、新制氯水? C、CaCl2溶液? D、次氯酸
参考答案:B
本题解析:A液氯只含有氯分子。
B、新制氯水既含有氯分子,也含有氯离子
C、CaCl2溶液只含有氯离子
D次氯酸既不含有氯分子,也不含有氯离子
本题难度:一般
4、选择题 如图所示,大试管里充满某混合气体,置于光亮处,将滴管里的水挤入大试管后,烧杯中的水会进入大试管,大试管里的气体可能是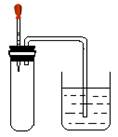
①N2、H2;②CO、O2; ③NO2、O2;④CH4、Cl2
A.①或③
B.②或④
C.①或③或④
D.③或④
参考答案:D
本题解析:烧杯中的水会进入大试管,说明大试管中气体体积减少,压强减小造成的;①N2和H2不反应;②CO和O2不反应;③NO2、O2和水能反应,气体体积减小;④CH4和Cl2在光照条件下,发生取代反应,生成液体氯代烃,气体体积减少;满足题意的是③或④,选D。
本题难度:一般
5、填空题 如图所示,将等物质的量的Cl2和CH4充入一容积为 25 mL的量筒,并将量筒倒置在盛有饱和食盐水的水槽中,用日光散射,可观察到的现象是;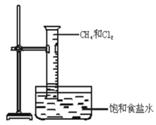
①?
②?
③?
④?
参考答案:气体的黄绿色变浅,最后为无色? 有油状液滴附着在量筒内壁
饱和食盐水中有晶体析出? 量筒内气体体积减小,液面上升
本题解析:在光照的条件下氯气和甲烷发生取代反应生成卤代烃和氯化氢,卤代烃不能溶于水,氯化氢极易溶于水,所以实验中可以观察到的实验现象是气体的黄绿色变浅,最后为无色;有油状液滴附着在量筒内壁;饱和食盐水中有晶体析出;量筒内气体体积减小,液面上升。
点评:该题是基础性试题的考查,试题基础性强,难易适中。侧重对基础知识的巩固和训练的,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生规范严谨的实验设计能力,也有助于调动学生的学习兴趣和学习积极性,提升学生的学科素养。
本题难度:一般