时间:2025-06-25 22:14:33
1、选择题 工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g) = Si(s)+4HCl(g) 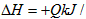 mol(Q>0) 某温度.压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是
mol(Q>0) 某温度.压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是
[? ]
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1mol,则达平衡时,吸收热量为QkJ
C.反应至4min时,若HCl浓度为0.12mol/L,则H2的反应速率为0.03mol/(L·min)
D.当反应吸收热量为0.025QkJ时,生成的HCl通入100mL 1mol/L的NaOH溶液恰好反应
参考答案:D
本题解析:
本题难度:一般
2、选择题 对可逆反应4NH3(g) + 5O2(g)  4NO(g) + 6H2O(g),下列叙述正确的是
4NO(g) + 6H2O(g),下列叙述正确的是
[? ]
A.达到化学平衡时,4υ正(O2) = 5υ逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大
D.化学反应速率关系是:2υ正(NH3) = 3υ正(H2O)时,达化学平衡状态
参考答案:A
本题解析:
本题难度:一般
3、选择题 在一密闭容器中,反应mA(g)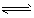 nB(g)达到平衡后,保持温度不变,改变容器体积(V)时,B的浓度变化如下图所示,以下判断正确的是
nB(g)达到平衡后,保持温度不变,改变容器体积(V)时,B的浓度变化如下图所示,以下判断正确的是
[? ]
A.平衡向逆反应方向移动
B.物质B的质量分数增加
C.物质A的转化率减小
D.化学计量数:m>n
参考答案:B
本题解析:
本题难度:一般
4、选择题 某温度下,在一容积可变的容器中,反应2A(g)+B(g)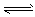 2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2 mol和4 mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是
2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2 mol和4 mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是
[? ]
参考答案:C
本题解析:
本题难度:一般
5、选择题 一定温度下,1 molX和n mol Y在体积为2L的密闭容器中发生如下反应:X(g)+Y(g)=2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z.下列说法正确的是( )
A.用X表示此反应的反应速率是(0.1-0.2a)mol?(L?min)-1
B.当混合气体的质量不再发生变化时,说明反应达到平衡状态
C.向平衡后的体系中加入1mol M,平衡向逆反应方向移动
D.向上述平衡体系中再充入1mol X,v(正)增大,v(逆)减小,平衡正向移动
参考答案:A.5min后达到平衡,生成2amolZ,则参加反应的X的物质的量为2amol×12=amol,故v(X)=amol2L5min=0.1amol/(L?min),故A错误;
B.随反应进行,反应混合气体的质量减小,混合气体的质量不变,说明到达平衡,故B正确;
C.因固体和纯液体改变它的物质的量并不会改变它的浓度,因此化学平衡并不移动,故C错误;
D.向上述平衡体系中再充入1molX,反应物的浓度增大,生成物的浓度不变,所以v(正)增大,v(逆)不变,平衡向正反应移动,故D错误;
故选B.
本题解析:
本题难度:简单