时间:2025-06-25 22:13:42
1、选择题 下列酸在与金属反应时,其中S元素或N元素的化合价不发生变化的是
[? ]
A.稀硫酸
B.浓硝酸
C.浓硫酸
D.稀硝酸
参考答案:A
本题解析:
本题难度:简单
2、选择题 根据有机物( )的结构,它不可能发生的反应是
)的结构,它不可能发生的反应是
A.水解反应
B.使溴的四氯化碳溶液褪色
C.与乙醇在浓硫酸催化下发生酯化反应
D.与碳酸钠溶液反应
参考答案:A
本题解析:略
本题难度:简单
3、填空题 (10分) 莽草酸具有抗炎、镇痛作用,还可作为合成抗病毒和抗癌药物的中间体。莽草酸可以实现下列转化:
已知:①
请回答下列问题。
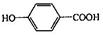
(1)A的结构简式是?。
(2)B C的化学方程式是
C的化学方程式是
?。
反应类型是?反应。
(3)在有机物分子中,若碳原子连接四个不同的原子或原子团,该碳原予称为手性碳原
子。E分子中手性碳原子有?个。
(4)莽草酸经过中间产物D合成E的目的是?。
参考答案:每空2分
(1)
(2)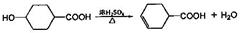 ?消去
?消去
(3)3
(4)防止羟基被氧化
本题解析:略
本题难度:简单
4、选择题 对金属锌与浓硫酸的反应来说,下列说法不当的是( )
A.若金属锌足量,反应所放出的气体应为混合物
B.反应消耗的锌的物质的量一定等于反应生成的气体的物质的量
C.由于金属铝的活动性强于锌,所以铝与浓硫酸的反应一定比锌与浓硫酸反应剧烈
D.反应中所转移的电子的物质的量一定等于反应生成的气体的物质的量2倍
参考答案:锌和浓硫酸反应方程式为:Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O、Zn+H2SO4=ZnSO4+H2↑,
A.锌和浓硫酸反应生成二氧化硫,随着反应的进行,浓硫酸变为稀硫酸时,二者反应生成氢气,所以生成的气体是混合物,故A正确;
B.根据Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O、Zn+H2SO4=ZnSO4+H2↑知,消耗锌的物质的量等于生成气体的物质的量,故B正确;
C.常温下,铝和浓硫酸发生钝化现象而阻止进一步反应,故C错误;
D.Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O、Zn+H2SO4=ZnSO4+H2↑中,转移电子和生成气体之间的物质的量之比=2:1,故D正确;
故选C.
本题解析:
本题难度:简单
5、选择题 “亲爱的水:每当我遇上你,我就有种沸腾的感觉。当我见不到你时,我甚至会在空气中寻找你的气息……’----这是浓硫酸对水的真情告白。图中小试管中盛有几毫升水,与大试管连通的U形细玻璃管内放有少量水(已染成红色)。如沿小试管壁小心地慢慢注入3 mL浓硫酸,静置片刻后,U形细玻璃管中可观察到的液面现象是 
[? ]
A.左高右低
B.左低右高
C.左右一样高
D.来回振动
参考答案:B
本题解析:
本题难度:简单