时间:2025-06-25 21:54:01
1、选择题 在盛有碘水的试管中,加入少量CCl4后振荡,静置片刻后( )
A.整个溶液变紫色
B.整溶液变为棕黄色
C.上层为无色下层为紫红色
D.下层无色上层紫红色
2、选择题 现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
[? ]
A.分液、萃取、蒸馏
B.萃取、蒸馏、分液
C.分液、蒸馏、萃取
D.蒸馏、萃取、分液
3、选择题 下列除去杂质的方法中正确的是(?)
A.用加热法除去Na2CO3固体中的NaHCO3
B.用加热法除去MnO2固体中的KMnO4
C.用加热法除去SiO2中的Na2SiO3
D.用加热法除去SiO2中的CaCO3
4、填空题 已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性。从溶液中将Cu2+、Fe2+、Fe3+沉淀为氢氧化物所需pH分别为6.4,6.4.3.7。现有某氯化铜晶体中含有FeCl2杂质,为制取纯净的CuCl2・2H2O,首先将其制成水溶液,然后按如图所示步骤进行提纯。 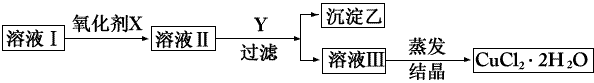
现有可供选择的试剂组(前X后Y):
A.H2O2、CuO B.KMnO4、Cu(OH)2 C.NaClO、CuO D.K2Cr2O7、CuCO3
回答下列问题:
(1)最适合本实验的试剂组是______________。
(2)加入氧化剂的目的是______________。
(3)本实验能否用加碱除去FeCl2?为什么?
_________________________________________________。
(4)最后能否直接蒸发结晶?若不能,应如何操作?
_________________________________________________。
5、选择题 2 molNa2CO3的质量是
A.53 g
B.106 g
C.212 g
D.53 g/mol