时间:2025-06-25 21:41:50
1、选择题 下列递变情况中,正确的是(? )
A.Na、Mg、Al原子的最外层电子数依次减少
B.Si、P、S元素的最高正价依次降低
C.C、N、O的原子半径依次减小
D.Li、Na、K的金属性依次减弱
参考答案:C
本题解析:A、Na、Mg、Al原子的最外层电子数分别为1、2、3依次增加;B、Si、P、S元素的最高正价分别为+4、+5、+6,依次增加;C、同周期元素的原子半径随着原子序数的递增而减小,故正确;D、同主族元素从上至下金属性逐渐增强。
本题难度:一般
2、选择题 2013年2月朝鲜进行了第三次核试验,引起国际社会的极大关注。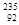 U是一种重要的核燃料,这里的“235”是指该原子的
U是一种重要的核燃料,这里的“235”是指该原子的
A.质子数
B.中子数
C.电子数
D.质量数
参考答案:D
本题解析:235是质量数,92是质子数。
本题难度:简单
3、选择题 元素X的原子核外第三层上有3个电子,元素Y的负二价离子核外有10个电子,则这两种元素形成化合物的化学式为(?)
A.XY2
B.X2Y3
C.X2Y
D.X3Y2
参考答案:B
本题解析:略
本题难度:简单
4、选择题 下列表示方法正确的是
A.铜的原子结构示意图: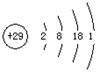
B.S2- 核外电子排布式:[Ne] 2s23p6
C.O原子处于基态的轨道表示式: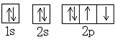
D.用电子式表示MgCl2的形成:Mg:+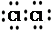 →
→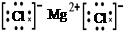
参考答案:A
本题解析:硫离子的最外层电子数是8个,B不正确;C不正确,不符合洪特规则;D不正确,应该是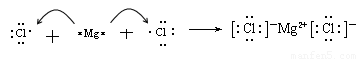 ,答案选A。
,答案选A。
本题难度:简单
5、填空题 (12分)现有6种短周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| W | 周期表中原子半径最小的元素 |
| U | 地壳中含量最多的金属元素 |
| R | 单质为空气的主要成分之一 |
| T | M层上有6个电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
参考答案:
小题1:16?14C?
小题2: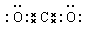 ?
?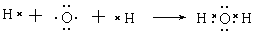
小题3: Cl? b
本题解析:考查原子核外电子的排布规律以及元素周期律的应用。周期表中原子半径最小的元素是H,则W是H。地壳中含量最多的金属元素是氧,则U是O。单质为空气的主要成分之一,则R是N。M层上有6个电子的元素是硫,则T是S。最外层电子数是次外层电子数的2倍的元素是碳,则X是C。氢化物水溶液呈碱性是氨气,则Y是N。元素最高正价是+7价短周期元素是Cl,则Z是Cl。
小题1:质子数等于核电荷数等于核外电子数,测定文物年代的是14C。
小题2:化合物XR2是CO2,形成的化学键是极性键,形成的化合物是共价化合物。W、R形成的10电子分子是水,含有的化学键是极性键。
小题3:比较非金属性强弱时可以元素周期律,也可以利于最高价氧化物的水化物的酸性强弱,或者是非金属单质和氢气化合的难易程度以及相应氢化物的稳定性,或者是非金属之间的相互置换能力等。
本题难度:一般