时间:2025-06-25 21:41:00
1、选择题 a、b、c、d是四种短周期的主族元素。a、b、d同周期,其中d的质子数最大;a、c同主族。a的原子结构示意图为: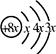 ;a与b形成化合物的电子式为:
;a与b形成化合物的电子式为: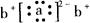 。
。
下列叙述正确的是(?)
A.原子半径:a>c>d
B.相应氢化物的沸点:d>c>a
C.非金属性:c>a>d
D.c与a、c与b均能形成两种常见化合物
2、选择题 据报道,2012年俄罗斯科学家再次合成117号元素。本次试验生成了6个新原子,其中5个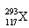 ,1个
,1个 。下列关于
。下列关于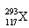 和
和 的说法,不正确的是
的说法,不正确的是
A.是两种核素
B.互为同位素
C.中子数分别为176和177
D.电子数相差1
3、选择题 锎(Cf)是非常有用的中子源,1 mg Cf每秒约放出8.34×109个中子,在医学上常用作治疗恶性肿瘤的中子源。下列有关锎的说法错误的是
A.Cf原子中,中子数为154
B.Cf原子中,质子数为98
C.Cf原子中,电子数为98
D.锎元素的相对原子质量为252
4、填空题 (14分)有A、B、C、D、E五种短周期主族元素,原子序数由A到E逐渐增大。
①A元素最外层电子数是次外层电子数的2倍。
②B的阴离子和C的阳离子与氖原子的电子层结构相同。
③在通常状况下,B的单质是气体,0.1molB的气体与足量的氢气完全反应共有0.4mol电子转移。
④C的单质在点燃时与B的单质充分反应,生成淡黄色的固体,此淡黄色固体能与AB2反应可生成B的单质。
⑤D的气态氢化物与其最高价含氧酸间能发生氧化还原反应。
请写出:
(1)A元素的最高价氧化物的电子式 ? 。
(2)B元素在周期表中的位置 ? 。
(3)B单质与C单质在点燃时反应的生成物中所含化学键类型有??。
(4)D元素的低价氧化物与E的单质的水溶液反应的化学方程式为______________。
(5)C与D能形成2:1的化合物,用电子式表示该化合物的形成过程的?。
(6)元素D与元素E相比,非金属性较强的是?(用元素符号表示),下列表述中能证明这一事实的是?(填选项序号)。
a.常温下D的单质和E的单质状态不同
b.E的氢化物比D的氢化物稳定
c.一定条件下D和E的单质都能与钠反应
d.D的最高价含氧酸酸性弱于E的最高价含氧酸
e.D的单质能与E的氢化物反应生成E单质
5、选择题 下列关于元素周期表中8号元素和16号元素的说法错误的是?(?)
A.具有相同的最外层 电子数? B
电子数? B .可以形成两种氧化物?
.可以形成两种氧化物?
C.位于同一周期? D.位于同一主族