时间:2025-06-25 21:36:06
1、选择题 25℃时,下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
A.在0.1?mol?L-1NH4Cl溶液中:c(NH4+)=c(Cl-)
B.在0.1?mol?L-1?NaHCO3溶液中:c(Na+)=c(HCO
参考答案:A、氯化铵中,铵根离子水解,但是氯离子不水解,所以c(NH4+)<c(Cl-),故A错误;
B、碳酸氢钠溶液中存在物料守恒:c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3),故B正确;
C、pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合后,醋酸会剩余,得到醋酸和醋酸钠的混合液中,离子浓度大小顺序是:c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故C错误;
D、在0.1?mol?L-1?Na2S溶液存在中质子守恒:c(OH-)=c(H+)+c(HS-)+2c(H2S),故D错误.
故选B.
本题解析:
本题难度:简单
2、简答题 根据Fe3++Ag?Fe2++Ag+,可用Fe3+的盐溶液做刻蚀液将试管中的银镜洗去.
(1)FeCl3溶液显酸性,原因是______(用离子方程式表示).
(2)关于FeCl3溶液洗银后的相关叙述正确的是______(填序号).
a.c(Fe3+)减小 b.?c(Cl-)不变 c.铁元素质量减小
(3)Fe(NO3)3溶液洗银时,甲同学认为NO3-也能将银氧化.他认为可以通过检验Fe(NO3)3溶液洗银后NO3-的还原产物来判断NO3-是否能将银氧化,而乙同学认为此方法不______可行,乙同学的理由是______.
(4)乙同学欲从洗银废液(Fe3+、Fe2+、Ag+、NO3-)中回收银和刻蚀液,设计了如下路线: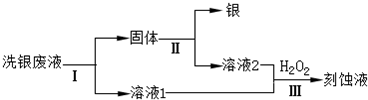
①过程Ⅰ中反应的离子方程式是______.
②过程Ⅱ中加入的试剂可以是______.
(5)镀银后的银氨溶液放置时会析出有强爆炸性的物质,所以不能贮存.从银氨溶液中回收银的方法是:向银氨溶液中加入过量盐酸,过滤,向沉淀AgCl中加入羟氨(NH2OH),充分反应后可得银,羟氨被氧化为N2.
①生成AgCl沉淀的化学方程式是______.
②若该反应中消耗3.3g羟氨,理论上可得银的质量为______g.
参考答案:(1)FeCl3溶液显酸性是因为铁离子水解生成氢氧化铁和氢离子;反应的离子方程式为:Fe3++3H2O?Fe(OH)3+3H+;
故答案为:Fe3++3H2O?Fe(OH)3+3H+;
(2)FeCl3溶液洗银,发生反应为:Fe3++Ag?Fe2++Ag+,
a.c(Fe3+)减小 故a符合;
b. c(Cl-)不变,故b不符合;
c.铁元素存在形式不同但质量不会减小,故c不符合;
故答案为:a;
(3)通过检验Fe(NO3)3溶液洗银后NO3-的还原产物来判断NO3-是否能将银氧化,需要在酸溶液中,亚铁离子也会反应;
故答案为:酸性条件下NO3-也可能与Fe2+发生氧化还原反应;
(4)①洗银废液(Fe3+、Fe2+、Ag+、NO3-)中回收银和刻蚀液需要先加入过量铁还原Fe3+、Ag+;反应的离子方程式为:2Fe3++Fe=3Fe2+Fe+2Ag+=Fe2++2Ag;
故答案为:2Fe3++Fe=3Fe2+Fe+2Ag+=Fe2++2Ag;
②过程Ⅱ中加入的试剂是溶解过量的铁,可以用稀盐酸或稀硫酸;
故答案为:稀盐酸或稀硫酸;
(5)①银氨溶液中加入过量盐酸生成氯化银,同时生成氯化铵和水,反应的化学方程式为:Ag(NH3)2OH+3HCl=AgCl↓+2NH4Cl+H2O;
故答案为:Ag(NH3)2OH+3HCl=AgCl↓+2NH4Cl+H2O;
②向沉淀AgCl中加入羟氨(NH2OH),充分反应后可得银,羟氨被氧化为N2.反应为:2AgCl+2NH2OH=N2↑+2Ag+2H2O+2HCl,反应中消耗3.3g羟氨物质的量=3.3g33g/mol=0.1mol;生成银物质的量为0.1mol,质量为10.8g;
故答案为:10.8;
本题解析:
本题难度:一般
3、选择题 有关①100ml 0.1 mol/LNaHCO3;②100ml 0.1 mol/LNaCO3两种溶液的叙述不正确的是?
[? ]
A.溶液中水电离出的个数:②>①
B.溶液中阴离子的物质的量浓度之和:②>①
C.①溶液中: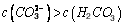
D.②溶液中: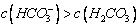
参考答案:C
本题解析:
本题难度:一般
4、选择题 已知某溶液中仅存在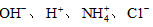 四种离子,其浓度大小有如下关系,其中一定不正确的是?
四种离子,其浓度大小有如下关系,其中一定不正确的是?
[? ]
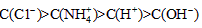
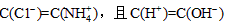
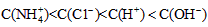
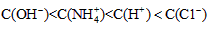
参考答案:C
本题解析:
本题难度:一般
5、选择题 下列物质的水溶液经加热浓缩,蒸干灼烧仍能得到原物质的是( )
A.FeCl3
B.Ca(HCO3)2
C.NaAlO2
D.Na2SO3
参考答案:C
本题解析:
本题难度:一般