时间:2025-06-25 21:35:17
1、实验题 (13分) 某研究性实验小组欲验证浓硝酸在与Cu、Ag合金的反应过程中除生成NO2气体外,还会有少量NO生成、并测定Cu、Ag合金中Cu的质量分数。查阅相关资料表明:“常温下,NO2与N2O4混合存在,在低于0℃时几乎只有无色的N2O4液体或晶体存在”。为此,他们设计了如下图所示的装置。回答下列问题: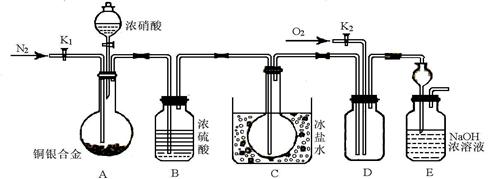
(1)写出A中Cu与HNO3反应可能的离子方程式?。?
(2)实验前先打开A部分的活塞K1,持续通一段时间的氮气再关闭K1,其目的是?;装置中B瓶的作用是?。
(3)停止反应后,打开D中的活塞K2并通入O2,若有NO生成,则D中出现的现象是?;实验发现,通入的O2温度高低对实验现象有较大影响,为便于观察应通入(填“热”或“冷”)?的O2。
(4)实验测得如下数据:实验前,Cu、Ag合金的质量:15.0g,浓HNO3:40mL 13.5 mol・L-1;实验后A溶液:V=40mL? c(H+)=1.0 mol・L-1。假设反应中HNO3 既无挥发也无分解,则:①参加反应的HNO3的物质的量为?mol?
②若已测出反应后E装置的生成物中含氮元素的质量m克,则为确定合金中Cu的质量分数还需测定的数据是?,若测得该数据为n,写出合金中铜的质量(设为x克)的求算式子(只需列式子,不需解方程)?。
(5)为减小上述实验误差,在D中观察到实验现象后还须进行的操作是?。
(6)若已知Cu、Ag合金的质量为m g,且溶解完全。只利用A装置中反应后的溶液进行简单的操作,也可以确定合金中Cu的质量分数,其实验操作过程为
?。
参考答案:(1)Cu+4H++ 2NO3-=Cu2++2NO2↑+2H2O?(1分)
3Cu+8H++ 2NO3-=3 Cu2++2NO↑+4H2O?(1分)
(2)把装置中的空气赶走,防止NO被氧化为NO2
(1分)干燥反应中生成的气体(1分)
(3)无色气体变为红棕色(1分)?热(1分)?(4)① 0.5(1分)
②C中烧瓶在实验前后增加的质量(1分)
2x/64+(15-x)/108=3m/14+n/46或2x/64+(15-x)/108="0.5-" m/14-n/46 (2分)
(5)打开K1、K2持续通入一段时间的N2和O2(1分)(不写N2不给分)
(6)在A中加入过量含Cl溶液,过滤后将沉淀洗涤、干燥,最后称取沉淀的质量(2分)
(不写过量扣1分,不写洗涤干燥扣1分)
本题解析:(1)浓硝酸的还原产物是NO2,但由于随着反应的进行,硝酸的浓度逐渐变稀,会生成NO,所以反应的方程式是Cu+4H++ 2NO3-=Cu2++2NO2↑+2H2O、
3Cu+8H++ 2NO3-=3 Cu2++2NO↑+4H2O。
(2)由于装置中含有空气,而空气能把NO氧化生成NO2,从而干扰实验的检验,所以这样操作的目的是赶走装置中的空气,防止干扰实验。由于生成的气体中含有水蒸气,而NO2能和水反应生成NO,从而无法确认铜与硝酸反应是否生成了NO气体,所以B装置的作用是干燥反应中生成的气体。
(3)NO极易被氧气氧化生成红棕色的NO2,所以实验现象是无色气体变为红棕色。由于存在可逆反应2NO2 N2O4,又因为该反应是放热反应,所以热的空气可以使平衡 2NO2
N2O4,又因为该反应是放热反应,所以热的空气可以使平衡 2NO2 N2O4向逆方向移动,因此NO2浓度增大,从而导致颜色加深,所以应该通入热的氧气。
N2O4向逆方向移动,因此NO2浓度增大,从而导致颜色加深,所以应该通入热的氧气。
(4) ①硝酸的总的物质的量是0.54mol,剩余硝酸是0.04mol,所以参加反应的硝酸是0.54mol-0.04mol=0. 5mol。
②要计算铜质量分数,还需要计算出生成的N2O4的质量。所以还需要测量C中烧瓶在实验
(5)由于装置中有残留的气体,所以在D中观察到实验现象后还须进行的操作是:打开K1、K2持续通入一段时间的N2和O2,以把气体完全排尽。
(6)由于反应后金属生成了硝酸盐,所以要测定该银圆中铜的质量分数,还需要把金属阳离子变成沉淀,然后通过称量即可计算,所以正确的操作可以是向反应后的溶液中加入足量的盐酸,过滤、洗涤、干燥、称量沉淀的质量。
点评:化学是一门以实验为基础的学科,所以有化学实验即科学探究之说法。化学实验主要以考察探究性实验和物质制备实验为主。这些探究性和制备性实验的试题,综合性强,理论和实践的联系紧密,有的还提供一些新的信息,要求学生必须认真审题,通过联系所学过的知识和技能,灵活运用并进行知识的类比、迁移、重组,全面细致的思考才能作出正确的解答。
本题难度:一般
2、填空题 (10分)(Ⅰ)将铜丝的一端绕成螺旋状,在酒精灯外焰加热,冷却后变黑。再在酒精灯上将该铜丝加热至红热状态。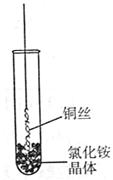
如右图所示,趁热插入到试管里的氯化铵晶体中,在试管中出现白烟。冷却后取出铜丝,可看到铜丝变成光亮的紫红色。回答下列问题:
⑴解释“当红热的铜丝插入氯化铵晶体中,出现白烟”的原因(用化学方程式表示)?。
⑵灼热的氧化铜在氯化铵中变成单质铜,写出该反应的化学方程式?。
( II)2008年,我国的航天事业取得了巨大的成就,航天员翟志刚顺利实现了太空行走。在航天发射时,肼(N2H4)及其衍生物常用作火箭推进剂。
⑴N2H4・H2O能发生类似NH3・H2O的微弱电离,使溶液显示弱碱性,该电离分两步,写出第一步电离的方程式?。
⑵在实验室中,用N2H4・H2O与NaOH颗粒一起蒸馏,收集114~116℃的馏分即为无水肼。①在蒸馏过程中不需要的仪器是?(填序号字母)。
A.酒精灯
B.长直玻璃导管
C.锥形瓶
D.冷凝管
E.牛角管(接液管)? F.蒸馏烧瓶? G.酸式滴定管
②除上述必需的仪器外,还缺少的玻璃仪器是?。
⑶肼能使锅炉内壁的铁锈(主要成分Fe2O3)变成磁性氧化铁(Fe3O4)层,可减缓锅炉锈蚀。若反应过程中肼转化为氮气,每生成1molFe3O4,需要消耗肼的质量为??g。
参考答案: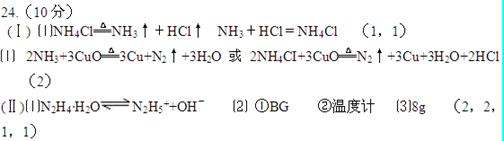
本题解析:略
本题难度:一般
3、选择题 为了科学地饮食,了解一些与食品相关的化学知识是必要的。
油炸虾条、薯片等容易挤碎的食品,不宜选用真空袋装,而应采用充气袋装。下列气体中最不应该充入的是(?)
A.氮气
B.二氧化碳
C.空气
D.氧气
参考答案:D
本题解析:食品袋内充氧气,易使食品氧化变质。
本题难度:简单
4、选择题 NO、NO2均可与NH3反应转化为无害的N2和H2O,现有3.0 L NO、NO2的混合气体,当耗用3.0 L NH3时,可全部转化为N2和H2O,则NO与NO2的体积之比为(体积均为同温、同压下测定)(? )
A.1∶1
B.1∶2
C.1∶3
D.任意比
参考答案:A
本题解析:存在4NO+5NH3====4N2+6H2O,6NO2+8NH3====7N2+12H2O反应,依据氧化还原反应的计算规则――化合价升高和降低的价态相等,知道NO与NO2的体积之比为1∶1,故A正确。
本题难度:简单
5、选择题 2008年奥运会将在北京举行,届时可能会用大型遥控飞艇作为宣传工具以渲染活动气氛,为了使飞艇在空中安全而有效,你认为飞艇内充入哪种气体最好()
A.氮气
B.氦气
C.氢气
D.二氧化碳
参考答案:B
本题解析:B 要同时考虑气体的密度和安全性。
本题难度:简单