时间:2025-06-25 21:23:01
1、选择题 “活化分子”是衡量化学反应速率快慢的重要依据,下列对“活化分子”的说法不正确的是
A.活化分子之间的碰撞一定是有效碰撞
B.增大反应物的浓度,可使单位体积内活化分子增多,反应速率加快
C.对于有气体参加的反应缩小体积,可使单位体积内活化分子增多,反应速率加快
D.催化剂能降低反应的活化能,使单位体积内活化分子百分数大大增加
2、计算题 在一定条件下,在容积为2L的密闭容器中,将2mol气体M和3mol气体N混合,发生如下反应:2M(g)+ 3N(g)  x Q(g)+3R(g),经2min达平衡,生成2.4molR,并测得Q的浓度为0.4mol/L。求:
x Q(g)+3R(g),经2min达平衡,生成2.4molR,并测得Q的浓度为0.4mol/L。求:
(1)用气体M来表示该反应的化学反应速率是多少?
(2)反应前后的压强比是多少?
(3)N的转化率是多少?
(4)平衡时气体Q所占的体积分数为多少?
3、填空题 (5分)⑴课本设计了如图一所示实验,其目的是通过比较H2O2的分解速率来比较 ,可通过观察 来定性比 较。有同学提出将CuSO4改为CuCl2更为合理,其理由是 。
较。有同学提出将CuSO4改为CuCl2更为合理,其理由是 。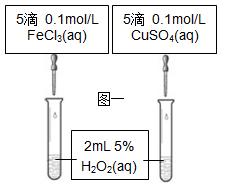
⑵已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。①针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是_____ 的影响。②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是_____
A.硫酸钾
B.硫酸锰
C.水
D.氯化锰
4、选择题 某化学兴趣小组欲探究反应物浓度对化学反应速率的影响,在保持其他条件都相同的情况下,使四份质量分数不同的H2O2溶液发生分解反应:2H2O2=O2↑+2H2O,其中氧气生成速率最大的是
A.5%H2O2溶液
B.10%H2O2溶液
C.20%H2O2溶液
D.30%H2O2溶液
5、填空题 (6分)在50mLH2O2水溶液中加入2g二氧化锰,在标准状况下放出气体的体积与时间的关系如右图所示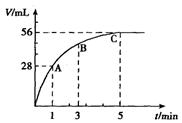
(1)该反应的化学方程式为?。?
(2)若溶液的体积保持50mL不变,则在前五分钟H2O2的平均反应速率为??mol/(L・min)。
(3)试解释A、B、C各点所表示的反应速率变化的原因?