时间:2025-06-25 21:13:08
1、选择题 如将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,即构成甲烷燃料电池。已知通入甲烷的一极,其电极反应为CH4+10OH―-8e- CO32―+7H2O,下列叙述正确的是
CO32―+7H2O,下列叙述正确的是
A.通入甲烷的一极为正极
B.通入氧气的一极发生氧化反应
C.该电池在工作时,溶液中的阴离子向正极移动
D.该电池总反应为CH4+2O2+2OH― CO32― +3H2O
CO32― +3H2O
2、计算题 (8分)氢氧燃料电池是将H2通入负极,O2通入正极而发生电池反应的,其能量转换率高。
(1)若电解质溶液为KOH,负极反应为_________________________________________
(2)若电解质溶液为硫酸,其正极反应为______________________?,若在常温下转移2mol电子,可产生水质量为_________g。
(3)若用氢氧燃料电池电解由NaCl和CuSO4组成的混合溶液,其中c(Na+)=3c(Cu2+)=3mol・L―1,取该混合液100mL用石墨做电极进行电解,通电一段时间后,在阴极收集到1.12L (标准状况)气体。此时氢氧燃料电池中消耗H2和O2的物质的量各是多少?(写出计算过程)(保留2位小数)
3、简答题 有些化学反应的化学能能直接转化成电能
I.利用Fe+CuSO4=FeSO4+Cu反应,设计一个原电池:
(1)在右框中画出装置图(标明电解质溶液、正、负极和电极材料)
(2)下列说法中,正确的是______.(填字母)
A.电解质溶液中阳离子向负极移动?B.电子通过外导线由负极流向正极
C.当导线中有1mol电子通过时,理论上正极放出1g气体
D.若所选电极的质量相等,理论上两极质量差为60g,导线中有1mol电子通过
II.三套装置如图所示,A、B、C烧杯中分别盛有相同物质的量浓度的稀硫酸.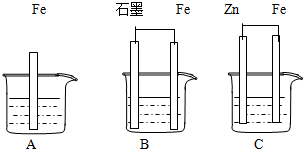
(1)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序为______;
(2)若C中电解质溶液是氯化钠溶液,则Fe电极的电极反应式为______;
III.目前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为:Cd+2NiO(OH)+2H2O?
?2Ni(OH)2+Cd(OH)2
已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸.
(1)以下说法中正确的是______①以上反应是可逆反应;?②以上反应不是可逆反应③充电时化学能转变为电能;④放电时化学能转变为电能.
(2)废弃的镍镉电池已成为重要的环境污染物,资料表明一节废镍镉电池可以使一平方米面积的耕地失去作用价值.在酸性土壤中这种污染特别严重,这是因为______
(3)另一种常用的电池是锂电池,锂是一种碱金属元素,其相对原子质量为7,由于它的比容量(单位质量电极材料所能转换的电量)特别大而广泛应用于心脏起搏器,一般使用时间可长达十年,它的负极用金属锂制成,电池总反应可表示为Li+MnO2=LiMnO2.
锂电池中的电解质溶液需用非水溶剂配制,为什么这种电池不能使用电解质的水溶液______(请用化学方程式表示其原因).
4、填空题 (8分)肼(N2H4)是火箭发射常用的燃料。一种以肼(N2H4)为燃料的电池装置如图所示。该燃料电池的电极材料采用多孔导电材料,以提高电极反应物在电极表面的吸附量,并使它们与电解质溶液充分接触,以空气中的氧气作为氧化剂,KOH溶液作为电解质。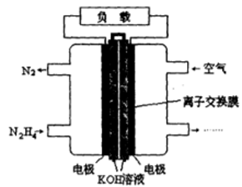
(1)负极上发生的电极反应为_________________;
(2)电池工作时产生的电流从_______电极经过负载后流向________电极(填“左侧”或“右侧”)。
(3)放电一段时间后,右侧溶液的pH (填“变大”或“变小”)
5、选择题 为体现“绿色奥运”“科技奥运”,2008年北京奥运会会出现中国自己生产的燃料电池汽车,作为马拉松领跑车和电视拍摄车,预计该车装着“绿色心脏”--质子交换膜燃料电池,其工作原理如图所示,下列叙述正确的是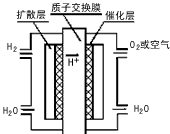
[? ]
A.通入氧气的电极发生氧化反应
B.通入氢气的电极为正极
C.总反应式为O2+2H2 2H2O
2H2O
D.正极的电极反应式为O2+4H++4e-==2H2O