ʱ��:2025-06-25 21:07:30
1������� ��8�֣���ֹˮ����Ⱦ������ˮ�ʣ�������Ĵ�ʩ�ǿ��ƹ�ҵ��ˮ��������ˮ���ŷš���һ�ֹ�ҵ��ˮ����֪���к��д�����Fe2+��SO42����������Ag+ �Լ��������ࡣijУ��ѧ��ȤС��ͬѧͨ�����в������̣��������ʣ�������ˮ��
���������������̣��ش��������⣺
�ο��𰸣���8�֣���1��©���ձ�������?��2�������ᾧ
��3��Fe? Fe+2Ag+=Fe2++2Ag?��4������������������
�����������1���������ǹ��ˣ���Ҫ����Ҫ����������©�����ձ�����������
��2�����ʴ���Һ����������Ҫ�����ᾧ��
��3��Ҫ���յ��������Ҳ������������ʣ���XӦ��������������Ӧ�����ӷ���ʽ��Fe+2Ag+=Fe2++2Ag��
��4������ת��ͼ��֪������B������������������������
�������������л��е����ʳ�ȥ����ô�������ᴿ���������һ��IJ�ͬ���ʱ˴˷ֿ����õ���Ӧ��ֵĸ�������з��롣�ڽ�����ʷ����ᴿ����ʱ,ѡ���Լ���ʵ���������Ӧ��ѭ����ԭ��: 1.���������µ����ʣ�ˮ���⣩���������ᴿ�������Ӧ�Ǵ����������Һ�����������������ʻ������У�2.�����ᴿ�������״̬���䣻3.ʵ����̺Ͳ������������У���ѡ������ᴿ����Ӧ��ѭ��������ѧ���ȼ��ӵ�ԭ��
�����Ѷȣ�һ��
2������� ����þ[Mg(ClO3)2]����������������ݼ��ȣ�ʵ�����Ʊ�����Mg(ClO3)2��6H2O���������£�
��֪��
��±����Ҫ�ɷ�ΪMgCl2��6H2O������MgSO4��FeCl2�����ʡ�
�ڼ��ֻ�������ܽ��(S)���¶�(T)�仯������ͼ��
��1����MgO�����������������Ҫ�ɷ�Ϊ?��
��2������BaCl2��Ŀ���dz�ȥSO42������μ���SO42���ѳ�����ȫ��?��
��3������NaClO3������Һ�ᷢ�����·�Ӧ��
MgCl2��2NaClO3 Mg(ClO3)2��2NaCl����
Mg(ClO3)2��2NaCl����
�����ø÷�Ӧ�������ͼ����ȡMg(ClO3)2��6H2O��ʵ�鲽������Ϊ��
��ȡ��������NaClO3������Һ��ַ�Ӧ����?����?����?���ݹ��ˡ�ϴ�ӣ����Mg(ClO3)2��6H2O���塣
��Ʒ��Mg(ClO3)2��6H2O�����IJⶨ��
����1��ȷ����3.50g��Ʒ�ܽⶨ�ݳ�100mL��Һ��
����2��ȡ10mL����ƿ�У�����10mLϡ�����20mL1.000mol/L��FeSO4��Һ���ȡ�
����3����ȴ�����£���0.100mol/LK2Cr2O7��Һ�ζ����յ㣬�˹����з�Ӧ�����ӷ���ʽΪ��Cr2O72����6Fe2����14H�� 2Cr3����6Fe3����7H2O��
2Cr3����6Fe3����7H2O��
����4��������2��3�ظ����Σ�ƽ������K2Cr2O7��Һ15.00mL��
��4��������Ʒ�ⶨ����Ҫ����Ƿ�©Һ��������?��
����3�����ζ�ǰ���ñ�Һ��ϴ�ζ��ܣ��ᵼ�����ս��ƫ?�������С������
��5����Ʒ��Mg(ClO3)2��6H2O����������Ϊ?��(������������λС��)
�ο��𰸣���1��BaSO4��Fe(OH)3?
��2�����ã�ȡ�ϲ���Һ����BaCl2�����ް�ɫ��������SO42��������ȫ������+�ж�1�֣�
��3���������ᾧ?�ڳ��ȹ���?�� ��ȴ�ᾧ?
��4������ƿ?�ζ���?ƫС
��5��78.31%
�����������1������ʵ���õ���������©�������������ձ�����ֽ������̨�ȣ����в��������У�©�������������ձ�����������þ��������Һ��pHΪ4����ʱ�������γ��˳��������������������Ѿ������������ֻ�Ӧ���������ᱵ�������ʴ�Ϊ��©�������������ձ���BaSO4��Fe��OH��3��
��2����������������Ƿ�����ķ��������ã�ȡ�ϲ���Һ����BaCl2�����ް�ɫ��������SO42��������ȫ���ʴ�Ϊ�����ã�ȡ�ϲ���Һ����BaCl2�����ް�ɫ��������SO42��������ȫ��
��3���������ʵ��ܽ�ȴ�С����Һ��þ���ķ����������ᾧ�����ȹ��ˣ���ȴ�ᾧ��
��4��������Ʒ�ⶨ����Ҫ����Ƿ�©Һ������������ƿ�͵ζ��� ������3�����ζ�ǰ���ñ�Һ��ϴ�ζ��ܣ��൱�ڰѱ�Һϡ���ˣ����ĵı�Һ������ͻ�ƫ�ߣ��ᵼ�����ս��ƫС��
��5������������Ӿ��������ԣ����Խ�������������Ϊ�����ۣ���ѧ����ʽΪ��ClO3��+6Fe2++6H+=6Fe3++Cl��+3H2O���ڸ��ݻ�ѧ����ʽ��ClO3��+6Fe2++6H+=6Fe3++Cl��+3H2O�Լ�Cr2O72��+6Fe2++14H+�T2Cr3++6Fe3++7H2O�����Եó���ClO3����6Fe2+��Cr2O72����6Fe2+����0.100mol?L��1 K2Cr2O7��Һ�ζ����յ���̿��Եó�ʣ����������ӵ����ʵ���Ϊ��0.100mol?L��1��0.015L��6=0.009mol������������ӷ�Ӧ���������ӵ����ʵ���Ϊ��20��10��3L��1.000mol?L��1��0.009mol=0.011mol����������ӵ����ʵ���Ϊ�� ��0.011mol����Ʒ��Mg��ClO3��2?6H2O��������������
��0.011mol����Ʒ��Mg��ClO3��2?6H2O�������������� ��0.011��299g/mol����10��
��0.011��299g/mol����10�� ��100%=78.3%���ʴ�Ϊ��78.3%��
��100%=78.3%���ʴ�Ϊ��78.3%��
�����Ѷȣ�һ��
3��ѡ���� ����0.1mol/L��NaCl��Һ�����в����ᵼ��������ҺŨ��ƫ�͵���
A.����ʱ�����̸ߣ����̵�?
B.����ʱ���Ӷ�ȡ�̶�?
C.ԭ����ƿϴ����δ����?
D.����ʱҺ�泬���˿̶���?
�ο��𰸣�D
���������������A����������ƽ����ҩƷʱ��ƽ���̷�ҩƷ�����̷����룻
B������ʱ���Ӷ�ȡ�̶ȣ���Һ��ʵ�����ƫС��?
C��ԭ����ƿϴ����δ�����ʵ������Ӱ�죻
D������ʱҺ�泬���˿̶��ߣ���Һ���ƫ��
��𣺸���c=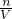 ��m=n��M�����жϣ�
��m=n��M�����жϣ�
A����������ƽ����ҩƷʱ��ƽ���̷�ҩƷ�����̷����룬����ʱ�����̸ߣ����̵ͣ�ҩƷʵ������ƫ��nƫ����cƫ��A��ѡ��
B������ʱ���Ӷ�ȡ�̶ȣ���Һ��ʵ�����ƫС��cƫ��B��ѡ��
C��ԭ����ƿϴ����δ�����ʵ������Ӱ�죬��C��ѡ��
D������ʱҺ�泬���˿̶��ߣ���Һ���ƫ��cƫС����Dѡ��
��ѡD��
���������⿼������һ�����ʵ���Ũ����Һ�ķ����������ѶȲ�������ʱ��c=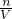 �ĽǶȷ���������������ҺŨ�ȵ�Ӱ�죮
�ĽǶȷ���������������ҺŨ�ȵ�Ӱ�죮
�����Ѷȣ���
4��ѡ���� ���г����ʵķ��������е���
[? ]
�ο��𰸣�A
���������
�����Ѷȣ�һ��
5��ѡ���� Ϊ��ȥ�����ڵ����ʣ���ѡ�õ��Լ�������ȷ����
[? ]
A��Na2CO3��Һ(NaHCO3)��ѡ������NaOH��Һ
B��NaHCO3��Һ(Na2CO3)��Ӧͨ�������CO2����
C��Na2O2��ĩ(Na2O)����������ڿ����м���
D��Na2CO3��Һ(Na2SO4)������������Ba(OH)2��Һ������
�ο��𰸣�D
���������
�����Ѷȣ�һ��