时间:2021-06-11 06:47:16
1、选择题 下列各组元素,按原子半径依次增大的顺序排列的是
A.C、N、O
B.N、S、Cl
C.P、S、Cl
D.Al、Mg、Na
2、填空题 下表列出前20号元素中的某些元素性质的一些数据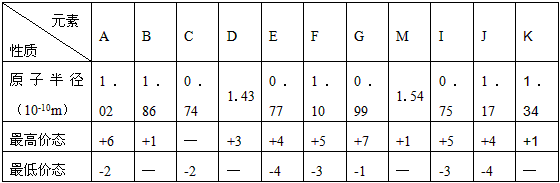
试回答下列问题
(1)以上11种元素中第一电离能最小的是_____________(填编号)。
(2)写出下列反应的化学方程式:M2C2与EC2反应__________________________。
(3)上述E、F、G三种元素中的某两种元素形成的化合物中,每一个原子都满足8电子稳定结构的是
__________(写一种分子式)。 比元素B原子序数大5的元素基态原子电子排布式是_____________。
(4)元素E与氢元素可形成分子式为E2H4的分子。其分子中E元素原子以________杂化成键,分子中共形成_______个σ键。
(5)C和I相比较,非金属性较弱的是_________(填元素名称),可以验证你的结论的是下列中的
_____________(填编号)。
a.气态氢化物的稳定性和挥发性
b.单质分子中的键能
c.两元素的电负性
d.含氧酸的酸性
3、选择题 X、Y、Z三种元素的原子,其最外层电子排布分别为ns1、3s23p1和2s22p4,由这三种元素组成的化合物的化学式可能是
[? ]
A.X3YZ3
B.X2YZ2
C.XYZ2
D.XYZ3
4、推断题 W、X、Y和Z都是周期表中前20号元素,已知:
①W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为WY的化合物;
②Y和Z属同族元素,它们能形成两种常见化合物;
③X和Z属同一周期元素,它们能形成两种气态化合物;
④W和X能形成组成为WX2的化合物;
⑤X和Y不在同一周期,它们能形成组成为XY2的化合物。
请回答:
(1)W元素是________;Z元素是_________。
(2)化合物WY和WX2的化学式分别是__________和___________。
(3)Y和Z形成的两种常见化合物的分子式是_________和_________。
(4)写出X和Z形成的一种气态化合物跟WZ反应的化学方程式_____________________。
5、选择题 下列各组单质中,前者能将后者从化合物中置换出来的是
①Al、Fe? ②H2、Cu? ③Mg、C? ④C、Na
A.只有①②?B.只有②③?C.只有①②③?D.①②③④