时间:2021-06-11 06:47:16
1、选择题 下表为元素周期表短周期的一部分。其中的一种元素E的原子的电子层数为n,最外层电子数为2n+1,原子核内质子数是2n2-1。下列有关A、B、C、D、E五种元素的叙述,不正确的是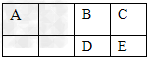
[? ]
A.A与B形成的阴离子可能有: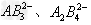 ?
?
B.D在过量的B中燃烧的主要产物为DB2
C.E的氢化物的沸点比C的氢化物的沸点高
D.D2E2分子中有极性键和非极性键
参考答案:C
本题解析:
本题难度:一般
2、选择题 下列元素中金属性最强的是( )
A.Na
B.K
C.Al
D.Si
参考答案:因Na、Al、Si均在第三周期,且原子序数依次增大,由同周期元素从左向右金属性在减弱,则三种元素金属性最强的为Na,
Na、K同主族,从上向下金属性在增强,所以金属性K>Na,所以四种元素金属性最强的是K.
故选B.
本题解析:
本题难度:一般
3、选择题 下列说法正确的是?
A.Fe 是地壳中含量最多的金属元素
B.钠在空气中燃烧的最终产物是Na2O
C.在 Al与NaOH溶液的反应中,Al是还原剂,H2O为氧化剂
D.铝箔在空气中受热可以熔化并滴落下来
参考答案:C
本题解析:略
本题难度:简单
4、推断题 A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为___________ ;其氢化物的水溶液显____________性。
(2)B元素的负二价离子和C元素的正二价离子的电子层结构都与氩相同,B的最高价氧化物的化学式为 ____________,C的元素符号为____________ ;
(3)D元素的正三价离子的3d亚层为半充满,D的元素符号为____________ ,其基态原子的电子排布式为_____________ 。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为 ____________,其基态原子的电子排布式为____________ 。
参考答案:(1)N; 碱
(2)SO3; Ca2+
(3) Fe; 1s22s22p63s23p63d64s2
(4)Cu ;1s22s22p63s23p63d104s1
本题解析:
本题难度:一般
5、简答题 下列是元素周期表的前三周期中的部分元素:
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 一 ① | ② 二 ③ ④ ⑤ ⑥ ⑦ 三 ⑧ ⑨ ⑩ (11) | |||||
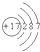 所表示的原子是______.(写元素符号)
所表示的原子是______.(写元素符号)参考答案:由元素在周期表中的位置可知,①为H、②为He、③为Li、④为C、⑤为N、⑥为O、⑦为F、⑧为Na、⑨为Mg、⑩为S、⑾为Cl,
(1)同周期自左而右非金属性最强、同主族自上而下非金属性减弱,故F元素最活泼;稀有气体He,最不活泼,故答案为:氟;氦;
(2)由原子结构示意图可知,该原子质子数为17,表示氯原子,故答案为:Cl;
(3)⑧和⑨两种元素的最高价氧化物对应的水化物分别为NaOH、Mg(OH)2,同周期自左而右金属性减弱,金属性Na>Mg,金属性越强,最高价氧化物对应的水化物的碱性越强,故碱性:NaOH>Mg(OH)2,故答案为:NaOH;Mg(OH)2;大于;
(4)上述第三周期元素中形成的离子化合物有NaCl等,故答案为:NaCl等.
本题解析:
本题难度:一般