时间:2021-06-11 06:45:27
1、选择题 可逆反应:aA(g)+bB(s) cC(g)+d D(g),当其他条件不变时,反应过程中某物质在混合物中的百分含量与温度(T)、压强(P)的关系如图所示,下列判断正确的是
cC(g)+d D(g),当其他条件不变时,反应过程中某物质在混合物中的百分含量与温度(T)、压强(P)的关系如图所示,下列判断正确的是
A.T1<T2 ΔH>0
B.T1>T2ΔH<0
C.P1<P2a=c+d
D.P1<P2a+b=c+d
参考答案:C
本题解析:
试题分析:当其他条件一定时,温度越高,反应速率越大,达到平衡所用的时间越短,由图象可知T2>T1,温度越高,平衡时C的百分含量(C%)越小,说明升高温度平衡逆移,故此反应的正反应为放热反应,即ΔH<0;当其他条件一定时,压强越高,反应速率越大,达到平衡所用的时间越短,由图象可知p2>p1;增大压强时B%不变,说明压强对平衡无影响,所以反应前后气体的计量数相等,即b=c+d,故C正确;故选:C.
考点:化学平衡图像
本题难度:一般
2、填空题 (16分)I.将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,各物质浓度随时间变化的关系如图1所示。
请回答:
(1)下列选项中不能说明该反应已达到平衡状态的是 (填选项字母)。
A.容器内混合气体的压强不随时间变化而改变
B.容器内混合气体的密度不随时间变化而改变
C.容器内混合气体的颜色不随时间变化而改变
D.容器内混合气体的平均相对分子质量不随时间变化而改变
(2)反应进行到10 min时,共吸收热量11.38 kJ,则该反应的热化学方程式为
;
(3)计算该反应的平衡常数K= 。
(4)反应进行到20 min时,再向容器内充入一定量NO2,10min后达到新的平衡,此
时测得c(NO2)="0.9" mol/L。
第一次平衡时混合气体中NO2的体积分数为w1,达到新平衡后混合气体中NO2的体积分数为w2,则w1 w2 (填“>”、“=”或“<”);
请在图2中画出20 min后各物质的浓度随时间变化的曲线(曲线上必须标出“X”和
“Y”)。
II.(1)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力。锂是制造化学
电源的重要原料。如LiFePO4电池中某电极的工作原理如下图所示:
该电池的电解质为能传导Li+的固体材料。放电时该电极是电池的 极(填“正”或“负”),该电极反应式为 。
(2)用此电池电解含有0.1 mol/L CuSO4和0.1 mol/L NaCl的混合溶液100 mL,假如电路中转移了0.02 mol e-,且电解池的电极均为惰性电极,阳极产生的气体在标准状况下的体积是__________L.
参考答案:Ⅰ.(1)B (2分)
(2)N2O4(g)  2NO2(g) △H="+56.9kJ/mol" (2分)
2NO2(g) △H="+56.9kJ/mol" (2分)
(3)0.9 (2分) (4)① > (2分) ②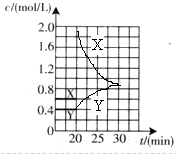 (2分)
(2分)
Ⅱ.正(2分) FePO4+e-+Li+=LiFePO4 (2分) 0.168 (2分)
本题解析:Ⅰ.(1)A、反应前后气体的化学计量数之和不等,故容器总压强不随时间改变可作为判断是否达到化学平衡状态的依据,正确;B、总质量不变,体积也不变,故混合气体的密度不随时间变化而改变不能作为判断是否达到化学平衡状态的依据,错误;C、NO2为红棕色气体,N2O4为无色气体,故混合气体的颜色不随时间变化而改变可作为判断是否达到化学平衡状态的依据,正确;D、总质量不变,总物质的量在变,故反应混合气平均分子量不再改变可作为判断是否达到化学平衡状态的依据,正确。
(2)由图1可知,反应物为N2O4,生成物为NO2,反应进行到10min时,N2O4的物质的量变化为0.2mol/L×1L=0.2mol,共吸收热量11.38kJ,故反应1molN2O4共吸收热量11.38×5=56.9kJ,故该反应热化学 方程式为:N2O4(g)?2NO2(g),△H=+56.9kJ?mol?1。
(3)k= c2(NO2)/ c(N2O4) =0.62÷0.4=0.9。
(4)①恒容,充入一定量NO2,相当于增大压强,平衡逆向移动,新平衡后混合气体中NO2的体积分数减小,故W1>W2。
②30min时,c(NO2)=0.9mol/L,k=0.92 ÷c(N2O4) =0.9,c(N2O4)=0.9mol/L,20min-30min,N2O4的浓度增加了0.9-0.4=0.5mol/L,故NO2的浓度减少了1mol/L,则20min时,c(NO2)=1+0.9=1.9mol/L,可画出20 min后各物质的浓度随时间变化的曲线。
Ⅱ.(1)放电时,该装置是原电池,Fe元素化合价由+3价变为+2价,得电子发生还原反应,所以该电极是正极,电极反应式为FePO4+e-+Li+=LiFePO4。
(2)计算得到,电解含有0.01mol CuSO4和0.01molNaCl的混合溶液100mL,电路中转移了0.02mol e-,
阳极:2Cl- -2e- =Cl2↑,
0.01mol 0.01mol 0.005mol
4OH--4e-=2H2O+O2↑,
0.01mol 0.01mol 0.0025mol所以阳极上生成的气体在标准状况下的体积=(0.005mol+0.0025mol)×22.4L/mol=0.168L。
考点:本题考查图像的分析及绘画、化学平衡状态、化学平衡常数、热化学方程式、原电池原理及应用。
本题难度:困难
3、填空题 生物质资源是一种污染小的可再生能源。生物质的主要转化途径及主要产物如下图。
(1)下列有关说法正确的是______________。
a.生物质能,本质上能量来源于太阳能
b.由纤维素水解获得的乙醇属生物质能
c.生物质裂解获得的汽油、柴油等属于纯净物
d.由植物秸杆等发酵获得的沼气,主要成是甲烷
(2)由生物质能获得的CO和H2,当两者1∶1催化反应,其原子利用率达100%,合成的物质可能是
______________。
a.汽油 b.甲醇 c.甲醛 d.乙酸
(3)已知在生物质气化炉中可发生:
C(s) + CO2(g) = 2CO(g) △H= 172kJ/mol
CH4(g)+ H2O(g) = CO(g) + 3H2(g) △H= 206kJ/mol
CH4(g)+ 2H2O(g) = CO2(g) + 4H2(g) △H= 165kJ/mol
则:C(s) + H2O(g) = CO(g) + H2(g) △H=__________kJ/mol。
(4)已知碳的气化反应在不同温度下平衡常数的对数值(lgK)如下表
反应:CO(g)+H2O(g) CO2(g)+H2(g),该反应的△H________0(选填:“>”、“<”、“=”);在900K时,该反应平衡常数的对数值(lgK)=_____________。
CO2(g)+H2(g),该反应的△H________0(选填:“>”、“<”、“=”);在900K时,该反应平衡常数的对数值(lgK)=_____________。
参考答案:(1)abd?
(2)cd?
(3)131
(4)<;0.36
本题解析:
本题难度:一般
4、选择题 在一定温度下的定容密闭容器中,当下列物理量不再改变时,表明反应:A(s)+2B(g) C(g)+D(g) 已达平衡标志的是
C(g)+D(g) 已达平衡标志的是
[? ]
参考答案:B
本题解析:
本题难度:一般
5、填空题 (15分)氨是最重要的氮肥,是产量最大的化工产品之一。课本里介绍的合成氨技术叫哈伯法,是德国人哈伯在1905年发明的,其合成原理为:N2(g)+3H2(g) 2NH3(g);△H<0他因此获得了1918年诺贝尔化学奖。工业上合成氨的部分工艺流程如下:
2NH3(g);△H<0他因此获得了1918年诺贝尔化学奖。工业上合成氨的部分工艺流程如下:
| 气体 | 氮气 | 氢气 | 氨 |
| 熔点(℃) | -210.01 | -252.77 | -77.74 |
| 沸点(℃) | -1 95.79 95.79 | -259.23 | -33.42 |
 (1)操作的目的:
(1)操作的目的:  2NH3(g),在673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是
2NH3(g),在673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是
参考答案:
本题解析:略
本题难度:困难