时间:2021-06-11 06:15:50
1、选择题 已知N2(g)+3H2(g) 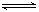 NH3(g)△H <0 ,SO2(g)+02(g)
NH3(g)△H <0 ,SO2(g)+02(g) 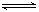 2S03(g),△H <0,不能用化学平衡移动原理说明的事实是
2S03(g),△H <0,不能用化学平衡移动原理说明的事实是
A.合成氨应该在高压塔中下进行
B.工业生产中,温度越低越好
C.制取SO2中,O2适当过量,经济性好
D.及时向合成氨气的塔里喷水,溶解、分离出氨气
参考答案:B
本题解析:
A.在合成NH3的可逆反应中,加压有利于平衡正移。
B.温度低虽然有利于两个平衡正移,提高转化率,但是温度低,速率太慢,生产效率低下。
C.制取SO2中,SO2价格贵,O2适当过量,SO2转化率大,经济性好
D.及时分离从合成塔中混合气体中的氨气,有利于合成氨
考点:1、影响化学反应速率的因素 2、影响化学平衡的因素
本题难度:一般
2、填空题 (1)对于下列反应:2SO2?+?O2 2SO3,?如果2min内SO2的浓度由6?mol/L下降为2?mol/L,那么,用SO2浓度变化来表示的化学反应速率为____________,用O2浓度变化来表示的反应速率为_____________。
2SO3,?如果2min内SO2的浓度由6?mol/L下降为2?mol/L,那么,用SO2浓度变化来表示的化学反应速率为____________,用O2浓度变化来表示的反应速率为_____________。
(2)下图表示在密闭容器中反应:2SO2+O2 2SO3?△H<0?
2SO3?△H<0?
达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况。 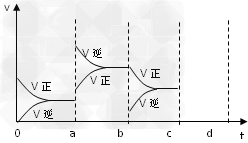
①ab过程中改变的条件可能是____________________;
②bc过程中改变的条件可能是____________________;?
③若加入催化剂,请将反应速度变化情况画在c~d处。
(3)请用化学平衡移动知识解释久置的氯水(尤其是长期放置在见光环境),最后浅黄绿色消失,溶液变成稀盐酸_________________。?
参考答案:(1)2mol/(L min);?1mol/(L
min);?1mol/(L min)?
min)?
(2)①升温;②减小?SO3浓度 ③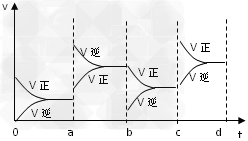 (3)在氯水中存在平衡:Cl2+H2O
(3)在氯水中存在平衡:Cl2+H2O HCl?+?HClO,HClO见光易分解为HCl和O2,使得平衡体系中HClO浓度减小,平衡向正反应方向移动,Cl2浓度减小、HCl浓度增大、最后浅绿色消失,溶液变成稀盐酸。
HCl?+?HClO,HClO见光易分解为HCl和O2,使得平衡体系中HClO浓度减小,平衡向正反应方向移动,Cl2浓度减小、HCl浓度增大、最后浅绿色消失,溶液变成稀盐酸。
本题解析:
本题难度:一般
3、选择题 汽车尾气净化中的一个反应如下:NO(g)+CO(g) 1/2N2(g)+CO2(g) △H=-373.4kJ·mol-1。 在恒容的密闭容器中,反应达到平衡后,改变某一条件,下列示意图正确的是
1/2N2(g)+CO2(g) △H=-373.4kJ·mol-1。 在恒容的密闭容器中,反应达到平衡后,改变某一条件,下列示意图正确的是
[? ]
A.
B.
C.
D.
参考答案:C
本题解析:
本题难度:一般
4、选择题 反应N2O4(g) 2NO2(g) ΔH=+57kJ/mol,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
2NO2(g) ΔH=+57kJ/mol,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是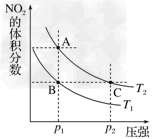
[? ]
A.A、C两点的NO2的体积分数:C>A
B.A、C两点气体的颜色:A深,C浅
C.由状态B到状态A,可以用加热的方法
D.若p2>p1,则化学平衡常数KA>KC
参考答案:C
本题解析:
本题难度:一般
5、选择题 向甲、乙两个容积均为1L的恒容容器中分别充入2mol?A、2molB和1molA、l?mol?B.
相同条件下发生如下反应:A(g)+B(g)?xC(g)△H<0.测得两容器中c(A)随时
间t的变化如图所示。下列说法错误的是( ? )
A.x可能等于2也可能等于3
B.若向平衡后的乙容器中充入C,则再次达到平衡时A?的体积分数增大
C.单独升高甲容器的温度,可使甲容器中各物质的体积分数与乙容器相同
D.若其它条件不变,使乙容器体积变为2L,则平衡时乙容器中:0.25mol?L-1<c(A)<0.5mol?L-1
参考答案:AB
本题解析:
本题难度:一般