时间:2021-06-11 06:13:22
1、选择题 对达到平衡的可逆反应X+Y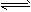 W+Z,增大压强则正、逆反应速率(v)的变化如图,分析可知X,Y,Z,W的聚集状态可能是
W+Z,增大压强则正、逆反应速率(v)的变化如图,分析可知X,Y,Z,W的聚集状态可能是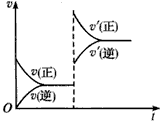
[? ]
A.Z,W为气体,X,Y中之一为气体
B.Z,W中之一为气体,X,Y为非气体
C.X,Y,Z皆为气体,W为非气体
D.X,Y为气体,Z,W中之一为气体
2、选择题 将4 mol M气体和2 mol N气体在2L的密闭容器中混合,并在一定条件下发生如下反应:2M(g)+N(g) 2Q(g)△H<0;4s后反应达到平衡状态,此时测得Q的浓度为0.6 mol/L。下列说法正确的是
2Q(g)△H<0;4s后反应达到平衡状态,此时测得Q的浓度为0.6 mol/L。下列说法正确的是
[? ]
A.当M、N、Q的物质的量浓度之比为2:1:2时,反应即达到平衡状态
B.4 s内用物质N表示的反应速率为0.075 mol・L-1・s-1
C.达到平衡后若通入一定量氦气,M的转化率降低
D.达到平衡后若升高温度,Q的浓度将增大
3、填空题 (10分)1000℃时,硫酸钠可与氢气发生反应: Na2SO4(s)+4H2(g)  Na2S(s)+4H2O(g)。请回答下列问题:
Na2S(s)+4H2O(g)。请回答下列问题: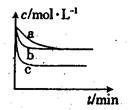
(1)上述反应的平衡常数表达式为: 。
(2)上述反应在三个不同条件下进行,与曲线a比较,b和c分别仅改变一种反应条件,其中H2的浓度随时间的变化如图所示。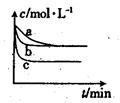
①则曲线b改变的条件为
②该反应的△H___0(填“>”、“<”或“=”)。
(3)该温度下,向2 L盛有1.42 g Na2SO4的密闭恒容容器中通入H2,5 min
后测得固体质量为1.10 g。
①则该时间范围内的平均反应速率v(H2)= 。
②能说明该反应已达到平衡状态的是 (填字母,下同)。
A.容器内压强保持不变
B.容器内气体密度保持不变
C.c(H2)=c(H2O)
D.v正(H2)=v逆(H2O)
4、填空题 (10分)已知A(g)+B(g)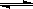 C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
| |温度/ ℃ | 700 | 900 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
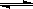 A(g)+B(g)的平衡常数的值为 。
A(g)+B(g)的平衡常数的值为 。 5、选择题 在一定条件下,密闭容器中发生可逆反应2X(g)+2Y(g) 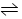 3Z(g)+2W(g),该X、Y的初始浓度分别为2.5 mol・L-1和2.0 mol・L-1,达平衡后,测出下列各生成物的浓度数据中肯定错误的是
3Z(g)+2W(g),该X、Y的初始浓度分别为2.5 mol・L-1和2.0 mol・L-1,达平衡后,测出下列各生成物的浓度数据中肯定错误的是
A.c(Z)="1.5" mol・L-1
B.c(Z)="2.4" mol・L-1
C.c(W)="1.6" mol・L-1
D.c(W)="2.0" mol・L-1