ʱ��:2021-06-11 06:09:04
1��ѡ���� �����������������������Ҫ��������Դ����ʽ������صķ����ǻ�ѧ�������һ���ش��ף������йص�ص���������ȷ���ǣ�������
A���ֻ����õ�����ӵ�����ڶ��ε��
B��п�̸ɵ���У�п�缫�Ǹ���
C��ͭпԭ��ع���ʱ�����������·��ͭ�缫����п�缫
D���״�ȼ�ϵ�ؿɰѻ�ѧ��ת��Ϊ����
�ο��𰸣�A������ӵ��Ϊ�ɳ���أ�Ϊ���ε�أ���ѭ��ʹ�ã���A��ȷ��
B��п�̸ɵ���У�пΪ������̼��Ϊ��������B��ȷ��
C��ͭпԭ��ع���ʱ��ͭΪ������пΪ���������ӴӸ��������·������������C����
D��ԭ���Ϊ��ѧ��ת��Ϊ���ܵ�װ�ã��״�ȼ�ϵ�ؿɰѻ�ѧ��ת��Ϊ���ܣ���D��ȷ��
��ѡC��
���������
�����Ѷȣ�һ��
2��ѡ���� ����ȼ�ϵ�������ں���ɻ��������Բ����缫��KOH��Һ������ʣ�������������ȷ���ǣ�?��
A��H2�ڸ�������������Ӧ
B��ȼ�ϵ�ص�����ת���ʿɴ�100%
C������Ϊ����Ⱦ��ˮ�����ڻ����Ѻõ��
D������ʱ���ܷ�ӦΪ��2H2 + O2 = 2H2O
�ο��𰸣�B
�����������������ȼ�ϵ�ص��ܷ�ӦΪ��2H2 + O2 = 2H2O����������Ⱦ������Ѻõ��
������O2��2H2O��4e��=4OH������ԭ��Ӧ��?������H2��2e����2OH��=2OH����������Ӧ��
���κ�����ת��������ģ�ת���ʲ����ܴ�100%���ʴ�ΪB
�����Ѷȣ���
3������� (9��) �۲����м���װ��ʾ��ͼ���й�������ȷ����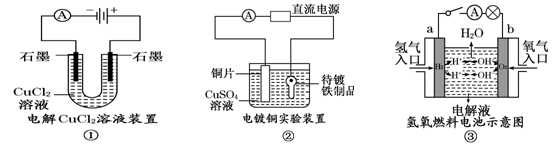
��1���ڢ�ͼ�У�������Ӧ�Ļ�ѧ����ʽΪ�� ��
��2���ڢ�ͼ�У���������ƷӦ���Դ ���������缫��ӦʽΪ�� ��
��3���ڢ�ͼ��,���·������ ������ ���������ҺΪKOH��Һ����b���ķ�ӦʽΪ ��
�ο��𰸣���1��CuCl2 Cu + Cl2��(2��) ��2����(1��) Cu2++2e�� = Cu (2��)
Cu + Cl2��(2��) ��2����(1��) Cu2++2e�� = Cu (2��)
��3��a(1��) b (1��) O2 + 4e�� + 2H2O = 4OH��(2��)
�����������1��װ�â��������������ӷŵ�����������������ͭ���ӷŵ�����ͭ�����Է�����Ӧ�Ļ�ѧ����ʽΪCuCl2 Cu+Cl2������2��װ�âڵĴ�������ƷӦ���Դ�����������缫��ӦʽΪ��Cu2++2e-=Cu����3��װ�â��У�a�缫�Ǹ�����b�缫������������������ʧ���ӣ������������õ��ӣ����Ե��Ӵ�a���ص�������b������ӦʽΪO2+4e-+2H2O=4OH-��
Cu+Cl2������2��װ�âڵĴ�������ƷӦ���Դ�����������缫��ӦʽΪ��Cu2++2e-=Cu����3��װ�â��У�a�缫�Ǹ�����b�缫������������������ʧ���ӣ������������õ��ӣ����Ե��Ӵ�a���ص�������b������ӦʽΪO2+4e-+2H2O=4OH-��
���㣺����ԭ��غ͵��صĹ���ԭ����
�����Ѷȣ�һ��
4��ѡ���� ����ijδ֪��Һ���Ƿ���SO�����в������������(����)
A���ȼ�ϡ�����ữ���ټ���Ba(NO3)2��Һ[
B����BaCl2��Һ����
C���ȼ������ữ���ټ�BaCl2��Һ
D����Ba(NO3)2��Һ����
�ο��𰸣�C
���������A��������Һ����SO32-��Ҳ����������B������BaCl2��Һ���ɵij��������������ơ�̼�ᱵ���Ȼ����ȣ�C��ȷ���ȼ�ϡ�����ữ���ų��������ӵĸ��ţ��ټ��Ȼ��������а�ɫ�������ɣ���һ������������ӣ�D���������ᱵ��Ӧ���ɵij�����һ�������ᱵ��
�����Ѷȣ���
5��ѡ���� ���������ҺΪ��������ˮ��Һ������ȼ�ϵ�ص�ⱥ��̼������Һһ��ʱ�䣬������ʱ�¶Ȳ������ö��Ե缫������˵����ȷ����( ��)
A������ظ�������m g����ʱ����������ͬʱ��m g��������
B����صĸ�����ӦʽΪ��O2��2H2O��4e-=4OH-
C������c(Na2CO3)���䣬����Һ���о�������
D��ȼ�ϵ����c(KOH)���䣻��������ҺpH���
�ο��𰸣�C
���������A��������ӦΪ��H2��2e���T2H+����H2+2e��+2OH-�TH2O������������mg����ʱ��ת�Ƶĵ��ӵ����ʵ���Ϊmg ��2g/mol �� 2= mmol�����������ĵ���Ϊmmol��������ӦΪ��2H++2e���TH2���������������������Ϊm�� 2 mol��2g/mol=mg����A����
B����ص�������ӦʽΪ��O2��2H2O��4e-=4OH-����B����
C�����ݵ缫����ʽ��֪���Na2SO4ˮ��Һʵ���ǵ���ˮ������Na2SO4ˮ�ܵ�Ũ�Ȳ��䣬����Һ���о�����������C��ȷ��
D��ȼ�ϵ�ص��ܷ�ӦΪO2+2H2�T2H20��ԭ�����c��KOH����С��������ҺpH��С����D����
��ѡC��
���������⿼��ԭ��غ͵���֪ʶ������ע��缫����ʽ����д��Ϊ���ô�����Ŀ�Ĺؼ�֮����
�����Ѷȣ���