时间:2021-06-11 06:06:33
1、选择题 常温下,下列各组微粒在指定溶液中一定能大量共存的是
A.0.1 mol・L-1 Fe(NO3)3溶液中:Mg2+、H+、SO42-、Cl-
B.0.1 mol・L-1 KClO溶液中:Na+、H+、Cl-、NO3-
C.0.1 mol・L-1氨水中:Ba2+、Ag+、NH4+、NO3-
D.c(OH-)=10-13 mol・L-1的溶液中:MnO4-、Na+、Br-、CH3CHO
2、选择题 某溶液中存在大量的Ba2+、Ag+、NH4+,该溶液中还可能大量存在的离子是
A.OH-
B.Cl-
C.SO42-
D.NO3-
3、填空题 (6分)将下列离子Na+、K+、Cu2+、H+、NO3-、Cl-、CO32-、OH-按可能大量共存于同一溶液的情况,把他们分成A、B两组,而且每组中均含两种阳离子和两种阴离子。
A组:?。
B组:?。
4、选择题 下列各组离子,在指定的环境中一定能大量共存的是
[? ]
A.在由水电离出的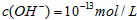 的溶液中:
的溶液中: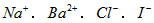
B.在加入铝粉能产生H2的溶液中: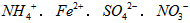
C.在能使pH试纸变深蓝色的溶液中: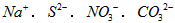
D.在pH为7的溶液中: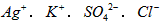
5、选择题 在T ℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g/cm3,溶质的质量分数为w,其中含NH4+的物质的量为b mol。下列叙述中正确的是(? )
A.溶质的质量分数为w=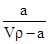 ×100%
×100%
B.溶质的物质的量浓度c=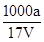 mol/L
mol/L
C.溶液中c(OH-)=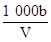 mol/L
mol/L
D.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w