时间:2021-06-11 06:03:42
1、选择题 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示.下列说法正确的是( )
| ? | ? ? ? X? Y ? ? Z ? ? W ? ? | ||||
参考答案:由元素在周期表的位置可知,Y为O元素、W为S元素、X为N元素、Z为Al元素;
A、Z为Al元素,处于第三周期第ⅢA族,故A错误;
B、同周期自左而右原子半径减小,电子层越多原子半径越大,所以原子半径的大小顺序为:rZ>rW>rX>rY,故B错误;
C、氧元素的氢化物有H2O2,故C错误;
D、O2-和Al3+核外电子数都是10,电子层数都是2,故D正确;
故选D.
本题解析:
本题难度:一般
2、填空题 已知A、B、C、D、E、F六种短周期元素的性质或结构信息如下表,请根据信息回答下列问题。
| 元素 | 性质或结构信息 |
| A | 单质常温下为固体,难溶于水易于溶CS2。能形成2种二元含氧酸。 |
| B | 原子的M层有1个未成对的p电子。核外p电子总数大于7。 |
| C | 单质曾被称为“银色的金子”。与锂形成的合金常用于航天飞行器。单质能溶强酸和强碱。 |
| D | 原子核外电子层上s电子总数比p电子总数少2个。单质和氧化物均为空间网状晶体,具有很高的熔、沸点。 |
| E | 其氧化物是汽车尾气的主要有害成分之一,也是空气质量预报的指标之一;该元素在三聚氰胺中含量较高。 |
| F | 周期表中电负性最大的元素 |
参考答案:(1)3s23p4(2分),14(1分)。(2)N,F (各1分,共2分)
20090116
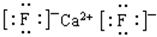 (2分)?
(2分)?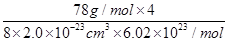 =3.2 g/cm3(列式2分,结果1分,无单位扣1分)
=3.2 g/cm3(列式2分,结果1分,无单位扣1分)本题解析:A、单质常温下为固体,难溶于水易于溶CS2,能形成2种二元含氧酸,因此A是S;B、原子的M层有1个未成对的p电子,核外p电子总数大于7,则B应该是Cl;C、单质曾被称为“银色的金子”,与锂形成的合金常用于航天飞行器,单质能溶强酸和强碱,所以C是Al;D、原子核外电子层上s电子总数比p电子总数少2个,单质和氧化物均为空间网状晶体,具有很高的熔、沸点,则D是Si;E、其氧化物是汽车尾气的主要有害成分之一,也是空气质量预报的指标之一;该元素在三聚氰胺中含量较高,则E是N;F、周期表中电负性最大的元素是F,即F是氟元素。
(1)S元素位于第三周期第ⅥA族,所以S原子的最外层电子排布式为3s23p4;Si元素的原子序数是14,核外电子数是14个,所以Si原子共有14种不同运动状态的电子。
(2)非金属性越强,第一电离能越大。但由于氮元素的2p轨道电子处于半充满状态,稳定性强,其第一电离能大于氟元素的,所以F与E元素第一电离能的大小关系:N>F。
(3)非金属性是S弱于Cl,所以两种元素的氢化物分子中键能较小的是H2S;非金属性越强,氢化物的稳定性越强,因此分子较稳定的是HCl。
(4)原电池中较活泼的金属做负极,镁的金属性强于Al。但由于铝能和氢氧化钠溶液,二镁不能,所以单质铝、镁、NaOH溶液构成的原电池中铝是负极,镁是正极,因此负极的电极反应式为Al-3e-+4OH- =AlO2-+2H2O。
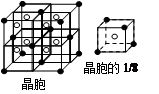
(5)根据晶胞的结构图并依据均摊原理可知,氟原子的个数=8个,钙原子的个数=8×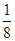 +6×
+6×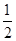 =4个,因此该化合物的化学式为CaF2,含有离子键的离子化合物,因此其电子式为
=4个,因此该化合物的化学式为CaF2,含有离子键的离子化合物,因此其电子式为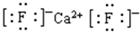 ;已知该化合物晶胞1/8的体积为2.0×10-23cm3,则该晶胞的体积是8×2.0×10-23cm3,因此根据晶胞中钙离子的个数是4个可知
;已知该化合物晶胞1/8的体积为2.0×10-23cm3,则该晶胞的体积是8×2.0×10-23cm3,因此根据晶胞中钙离子的个数是4个可知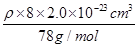 ×6.02×1023/mol=4,解得ρ=
×6.02×1023/mol=4,解得ρ=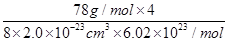 =3.2 g/cm3。
=3.2 g/cm3。
本题难度:一般
3、填空题 氯化铬酰(CrO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
请回答下列问题:
(1)写出铬原子的基态电子排布式________,与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有________(填元素符号),其中一种金属的晶胞结构如图所示,该晶胞中含有金属原子的数目为________。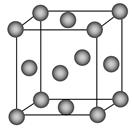
(2)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是________(填“极性”或“非极性”)分子。
(3)在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有________(填序号),CS2分子的空间构型是________。
参考答案:(1)1s22s22p63s23p63d54s1 K、Cu 4
(2)非极性 (3)①③ 直线形
本题解析:(1)铬元素是24号元素,处于第4周期,电子排布式为1s22s22p63s23p63d54s1,其最外层只有一个电子,同周期中原子最外层只有一个电子的元素还有K、Cu。根据晶胞图示可知,金属原子的数目为8×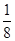 +6×
+6×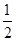 =4。
=4。
(2)CCl4、CS2均为非极性分子,根据相似相溶原理可知,CrO2Cl2为非极性分子。
(3)涉及含C的物质,若C都成单键为sp3杂化;共成一个双键则为sp2杂化;共成一个叁键和二个双键则为sp1杂化。
本题难度:一般
4、填空题 许多金属及它们的化合物在科学研究和工业生产中具有许多用途。
回答下列有关问题:
(1)基态Ni的核外电子排布式为__________________________________________,
第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是________。
(2)配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=________,CO与N2结构相似,CO分子内σ键与π键个数之比为________。
(3)NiO、FeO的晶体结构类型均与氯化钠的相同。
①Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO________FeO(填“<”或“>”);
②NiO晶体中Ni的配位数为________。
(4)金属Cu单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是________________________________________________________________________________________________________________________________________________,
反应的离子方程式为________________________________________________________________________。
(5)一种铜金合金晶体具有面心立方最密堆积的结构。在晶胞中,Au原子位于顶点,Cu原子位于面心,则该合金中Au原子与Cu原子个数之比为________,若该晶胞的边长为a pm,则合金的密度为________g・cm-3(只要求列算式,不必计算出数值,阿伏加德罗常数为NA)。
参考答案:(1)1s22s22p63s23p63d84s2 C(碳)
(2)4 1∶2
(3)①> ②6
(4)H2O2为氧化剂,氨与Cu2+形成配离子,两者相互促进使反应进行 Cu+H2O2+4NH3=Cu(NH3)42++2OH-
(5)1∶3 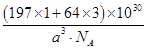
本题解析:(1)Ni基态原子中未成对电子数为2,与之未成对电子数相同的第二周期元素为碳元素和氧元素,电负性最小的为碳元素。(2)Ni原子价电子数为10,配体CO可以提供一个孤电子对,则n=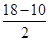 =4;氮氮三键中含有1个σ 键和2个π键,CO与N2结构相似,故CO分子内σ键与π键个数之比为1∶2。(3)①离子晶体中,在其他因素一样时,离子半径越小,离子键就越强,熔点越高;②NiO的晶体结构类型与氯化钠的相同,均为立方最密堆积,Ni原子与O原子的配位数均为6。(4)H2O2具有强氧化性,可以将Cu氧化为Cu2+,但反应速率很小,而氨与Cu2+形成配离子,两个反应相互促进使反应速率加快,反应得以进行。(5)Au原子位于顶点,则一个晶胞中含有Au原子数为8×
=4;氮氮三键中含有1个σ 键和2个π键,CO与N2结构相似,故CO分子内σ键与π键个数之比为1∶2。(3)①离子晶体中,在其他因素一样时,离子半径越小,离子键就越强,熔点越高;②NiO的晶体结构类型与氯化钠的相同,均为立方最密堆积,Ni原子与O原子的配位数均为6。(4)H2O2具有强氧化性,可以将Cu氧化为Cu2+,但反应速率很小,而氨与Cu2+形成配离子,两个反应相互促进使反应速率加快,反应得以进行。(5)Au原子位于顶点,则一个晶胞中含有Au原子数为8×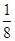 =1,Cu原子位于面心,则一个晶胞中含有Cu原子数为6×
=1,Cu原子位于面心,则一个晶胞中含有Cu原子数为6×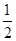 =3,故该合金中Au原子与Cu原子个数之比为1∶3;一个晶胞的质量为
=3,故该合金中Au原子与Cu原子个数之比为1∶3;一个晶胞的质量为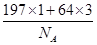 g,一个晶胞的体积为a3 pm3,故合金的密度为
g,一个晶胞的体积为a3 pm3,故合金的密度为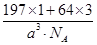 ?g・pm-3=
?g・pm-3=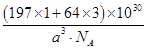 ?g・cm-3。
?g・cm-3。
本题难度:一般
5、选择题 对于 AZX和A+1ZX+两种粒子,下列叙述正确的是?
A.质子数一定相同,质量数和中子数一定不同
B.化学性质几乎相同
C.一定都由质子.中子.电子构成
D.核电荷数,核外电子数一定相同
参考答案:A
本题解析:略
本题难度:简单