时间:2021-06-11 06:02:16
1、选择题 某课外活动小组,为研究金属的腐蚀和防护的原理,做了以下实验:将剪下的一块镀锌铁片,放入锥形瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞试液,按如图所示的装置进行实验,过一段时间后观察.下列现象不?可能出现的是( )
A.B中导气管产生气泡
B.B中导气管里形成一段水柱
C.金属片剪口变红
D.锌被腐蚀
2、选择题 化学已渗透到人类生活的各个方面.下列说法不正确的是( )
A.阿司匹林具有解热镇痛作用
B.可以用Si3N4、Al2O3制作高温结构陶瓷制品
C.在入海口的钢铁闸门上装一定数量的铜块可防止闸门被腐蚀
D.禁止使用四乙基铅作汽油抗爆震剂,可减少汽车尾气污染
3、选择题 下列各装置中都盛有0.1 mol・L-1的NaCl溶液,放置相同时间后,锌片的腐蚀速率由快到慢的顺序是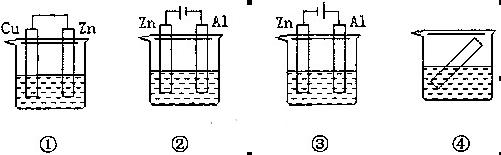
A.③①④②
B.①②④③
C.②①④③
D.②①③④
4、选择题 有一种纸质软电池,该电池采用薄层纸片作为载体和传导体,一面附着锌,另一面附着二氧化锰。电池总反应为Zn+2MnO2+H2O=ZnO+2MnO(OH),关于此电池,下列说法正确的是
A.该电池Zn为负极,ZnO为正极,MnO2催化剂]
B.该电池的正极反应为MnO2+e-+H2O=MnO(OH)+OH-
C.放电时外电路电子由Zn流向MnO2,内电路电子由MnO2流向Zn
D.电池工作时OH-通过薄层纸片向附着二氧化锰的电极移动
5、选择题 下列各方法中能对金属起到防止或减缓腐蚀作用的是
[? ]
①金属表面涂抹油漆 ②改变金属的内部结构 ③保持金属表面清洁干燥
④在金属表面进行电镀 ⑤使金属表面形成致密的氧化物薄膜
A.①②③④
B.①③④⑤
C.①②④⑤
D.全部