时间:2021-06-11 06:00:09
1、填空题 (1)向硫酸氢钠溶液中,逐滴加入Ba(OH)2溶液至中性。请写出发生反应的化学方程式: ;
(2)在以上中性溶液中,继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式 ;
参考答案:(1) Ba2++2OH-+2H++SO42-="=" BaSO4↓+2H2O ;(2分)
(2) Ba2+ +SO42-="=" BaSO4↓ 。(2分)
本题解析:略
本题难度:一般
2、选择题 下列表示对应化学反应的离子方程式正确的是
A.将过量SO2通入冷氨水中:SO2+NH3・H2O HSO3-+NH4+
HSO3-+NH4+
B.向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH- NH3↑+H2O
NH3↑+H2O
C.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O 3I2+6OH-
3I2+6OH-
D.用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3- Ag++NO↑+H2O
Ag++NO↑+H2O
参考答案:A
本题解析:A.将过量SO2通入冷氨水中:SO2+NH3・H2O HSO3-+NH4+,故A正确。B.漏掉了HCO3-与OH-的反应,故B错误。C.酸性溶液中不会生成OH-,故C错误。D.不符合电子守恒,故D错误。
HSO3-+NH4+,故A正确。B.漏掉了HCO3-与OH-的反应,故B错误。C.酸性溶液中不会生成OH-,故C错误。D.不符合电子守恒,故D错误。
考点:了解离子反应的概念、离子反应方程式的书写。
点评:离子方程式正误判断要在掌握基本方法的基础上,针对反应中物质的性质、反应的条件、物质的用量、反应的环境等因素具体分析,正确判断。特别是氧化还原反应的离子方程式书写一定符合“三守恒”:原子守恒,电荷守恒和电子守恒。
本题难度:一般
3、选择题 下列离子方程式书写正确的是( )
A.实验室用大理石和稀盐酸制取CO2:2H+ + CO32-= CO2↑+ H2O
B.稀盐酸与氢氧化钡溶液反应: H+ + OH- = H2O
C.硫酸镁溶液与氢氧化钡溶液反应:SO42- + Ba2+="=" BaSO4↓
D.铜与稀硫酸溶液反应:Cu + 2H+ = Cu2+ + H2↑
参考答案:B
本题解析:略
本题难度:一般
4、选择题 能正确表示下列反应的离子方程式是 ( )
A.向漂粉精溶液中通入过量的二氧化碳Ca2+ + 2ClO-+ H2O + CO2 = CaCO3↓+ 2HClO
B.金属钠与足量水反应 Na+2H2O=Na++H2↑+2OH-
C.碳酸氢钙溶液中加入足量烧碱溶液 HCO3-+OH-=CO32-+H2O
D.Cl2与水反应 Cl2+H2O=H++Cl-+HClO
参考答案:D
本题解析:A项二氧化碳过量生成HCO3-,B项电荷不守恒,C项生成的CaCO3难溶不能拆。答案选D。
考点:离子方程式正误判断
点评:离子方程式正误判断要注意:看是否符合客观事实、看是否符合质量守恒、看是否符合电荷守恒、看是否符合得失电子相等。可溶的易电离的物质拆成离子。注意过量、少量、适量等。
本题难度:困难
5、填空题 (12分)(1)环境专家认为可以用金属铝将水体中的NO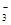 转化为N2,从而清除污染。该反应中涉及的粒子有:H2O、Al、OH
转化为N2,从而清除污染。该反应中涉及的粒子有:H2O、Al、OH 、Al(OH)3、NO
、Al(OH)3、NO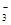 、N2,写出反应的离子方程式 。
、N2,写出反应的离子方程式 。
(2)我国首创的海洋电池以海水为电解质溶液,电池总反应为:4Al+3O2+6H2O=4Al(OH)3。电池正极的电极反应式为 。
(3)已知:4Al(s)+3O2(g)=2Al2O3(g) △H=-2834.9kJ/mol
Fe2O3(s)+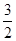 C(s)=
C(s)= 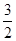 CO2(g)+2Fe(s) △H=+234.1kJ/mol
CO2(g)+2Fe(s) △H=+234.1kJ/mol
C(s)+O2(g)=CO2(g) △H=-393.5kJ/mol
写出铝与氧化铁发生铝热反应的热化学方程式 。
(4)将一定质量的钠铝合金置于水中,合金全部溶解,得到20mol,pH=14的溶液,然后2mol/L盐酸滴定,可得沉淀质量与消耗的盐酸体积关系如下图:则反应过程中产生氢气的总体积为 L(标准状况)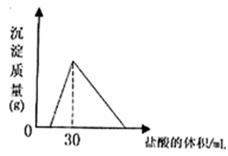
参考答案:(每空3分)(1)6NO3-+10Al+18H2O=10Al(OH)3+3N2↑+6OH- (2)2H2O+O2+4e-=4OH-
(3)2Al(s)+Fe2O3(s)==2Fe(s)+Al2O3(s)△H=-593.1kJ/mol; (4)2.016
本题解析:(1)由金属铝将水体中的NO3-转化为N2可知,反应中Al元素被氧化,化合价由0价升高到+3价;N元素被还原,化合价从+5价降低到0价,则根据电子得失守恒可知反应的离子方程式为6NO3-+10Al+18H2O=10Al(OH)3+3N2↑+6OH-;
(2)由电池总反应4Al+3O2+6H2O=4Al(OH)3可知,Al作负极,氧气在正极上得电子发生还原反应,正极反应为2H2O+O2+4e-=4OH-;
(3)由①4Al(s)+3O2(g)=2Al2O3(g)△H=-2834.9kJ/mol,②Fe2O3(s)+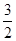 C(s)=
C(s)=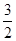 CO2(g)+2Fe(s)△H=+234.1kJ/mol,③C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol,根据盖斯定律可知,①×
CO2(g)+2Fe(s)△H=+234.1kJ/mol,③C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol,根据盖斯定律可知,①×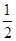 +②-③×
+②-③×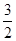 可得,2Al(s)+Fe2O3(s)=2Fe(s)=2Fe(s)+Al2O3(s)△H=-593.1kJ/mol;
可得,2Al(s)+Fe2O3(s)=2Fe(s)=2Fe(s)+Al2O3(s)△H=-593.1kJ/mol;
(4)由2Na+2H2O
本题难度:一般