1、实验题 2001年6月21日,河南的郑州、洛阳及南阳市率先使部分汽车采用封闭运行方式,试用新的汽车燃料――车用乙醇汽油。乙醇,俗名酒精,它是以玉米、小麦、薯类等为原料经发酵、蒸馏而制成的。乙醇进一步脱水,再加上适量汽油后形成变性燃料乙醇。而车用乙醇汽油就是把变性燃料乙醇和汽油按一定比例混配形成的车用燃料。结合有关知识,完成以下问题:
(1)乙醇的结构简式为_____________。汽油是由石油分馏所得的低沸点烷烃,其分子中的碳原子数一般在C5―C11范围内,如戊烷,其分子式为__________________,结构简式及其同分异构体分别为_____________、_____________、_____________。
(2)乙醇可由含淀粉〔(C6H10O5)n〕的农产品,如玉米、小麦、薯类等经发酵、蒸馏而得。请写出由淀粉制乙醇的化学方程式:
①淀粉+水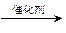 葡萄糖(C6H12O6)
葡萄糖(C6H12O6)
②葡萄糖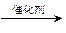 乙醇
乙醇
(3)淀粉可由绿色植物经光合作用等一系列生物化学反应得到,即水和二氧化碳经光合作用生成葡萄糖,由葡萄糖再生成淀粉。进行光合作用的场所是_____________,发生光合作用生成葡萄糖的化学方程式是
__________________________________________________________。
(4)乙醇充分燃烧的产物为__________________和__________________。
(5)车用乙醇汽油称为环保燃料,其原因是__________________________________________。
参考答案:(1)C2H5OH? C5H12? CH3―CH2―CH2―CH2―CH3?
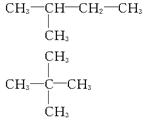
(2)①(C6H10O5)n+nH2O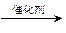 nC6H12O6
nC6H12O6
②C6H12O6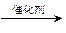 2C2H5OH+2CO2
2C2H5OH+2CO2
(3)叶绿体? 6CO2+6H2O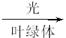 C6H12O6+6O2
C6H12O6+6O2
(4)CO2? H2O
(5)能有效降低汽车尾气带来的严重大气污染,改善环境质量
本题解析:本题是化学与生物相结合的题目,乙醇、汽油燃烧,生成CO2和水,不会对环境造成污染。
本题难度:简单
2、选择题 借助先进的实验仪器和方法,可测定有机化学分子结构和有机化学反应历程,下列实验方法主要用于测定有机化学反应历程的是
[? ]
A.同位素示踪法
B.核磁共振法
C.红外光谱法
D.质谱法
参考答案:A
本题解析:
本题难度:简单
3、选择题 研究物质性质的基本程序是一个系统化的过程,其主干可分为四个步骤.下列是研究物质性质的一般程序的第一步是( )
A.预测物质性质
B.观察物质的外观性质
C.进行实验和观察
D.做出有关的解释和结论
参考答案:B
本题解析:
本题难度:简单
4、选择题 下列有关化学研究的正确说法是(? )
A.化学家提出的假设不一定能被实验证实
B.同时改变两个变量来研究反应速率的变化,能更快得出有关规律
C.从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属性递增的规律
D.科恩和波普尔因理论化学方面的贡献获诺贝尔化学奖,标志着化学已成为以理论研究为主的学科,不需要再做化学实验
参考答案:A
本题解析:
本题难度:简单
5、填空题 某研究性学习小组用FeCl3溶液做“腐蚀液”,制作印刷电路板,其反应原理是:2FeCl3+Cu=2FeCl2+CuCl2。
【实验探究】
(1)通过《化学1》的学习,知道了有离子参加的化学反应为离子反应。离子反应可用离子方程式表示。请写出2FeCl3+Cu=2FeCl2+CuCl2反应的离子方程式为:?。
(2)若要溶解电路板上3.2g的铜,则至少需要FeCl3物质的量为?mol。
(3)使用后失效的“腐蚀液”为废液,验证废液中是否存在Fe3+的试剂是?,加入该试剂后,若出现?现象,说明废液中还存在Fe3+。
(4)废液中的CuCl2可通过加入足量的?,反应后转化成铜且能使所得溶液中含有单一溶质。
(5)回收Cu后的废液,通入足量的Cl2,可以重新获得FeCl3溶液,其反应的化学方程式为?。
【实验结论】
利用FeCl3溶液做印刷电路板的“腐蚀液”,不仅废液中的铜可以得到回收,经过处理后的废液还可以重新使用。
【知识拓展】
(6)铁元素是维持生命活动不可缺少的微量元素,虽然人体中通常只含有3~5g铁元素,但铁元素在人体中却发挥着重要作用,人体缺铁会引起?疾病。
参考答案:(13分)(1) 2Fe3+ + Cu=2Fe2+ + Cu2+?[2分]?(2)0.1 ?[2分]
(3)KSCN溶液(或NaOH溶液), 溶液呈(血)红色(或红褐色沉淀)?[每空2分(其它合理答案均得分)]
(4)铁粉?[2分]?(5)2FeCl2+Cl2=2FeCl3?[2分]?(6)贫血? [1分]
本题解析:(1)根据化学方程式可知,该反应的离子方程式是2Fe3+ + Cu=2Fe2+ + Cu2+。
(2)3.2g铜的物质的量是3.2g÷64g/mol=0.05mol,则根据反应的化学方程式可知,至少需要FeCl3物质的量为0.05mol×2=0.1mol。
(3)检验铁离子的方法是KSCN溶液或氢氧化钠溶液,实验现象是溶液呈(血)红色(或红褐色沉淀)。
(4)铁的金属性强于铜的,所以废液中的CuCl2可通过加入足量的铁粉,反应后转化成铜且能使所得溶液中含有单一溶质。
(5)氯气具有氧化性,能把氯化亚铁氧化,反应的离子方程式是2FeCl2+Cl2=2FeCl3。
(6)人体缺铁会引起贫血疾病。
点评:该题是高考中的常见题型和考点,属于基础性试题的考查,侧重对学生基础知识的巩固和训练,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力。也有利于调动学生的学习兴趣和学习积极性,提高学生灵活运用基础知识解决实际问题的能力。
本题难度:一般
微信搜索关注"91考试网"公众号,领30元,获取公务员事业编教师考试资料40G
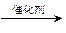 葡萄糖(C6H12O6)
葡萄糖(C6H12O6)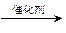 乙醇
乙醇
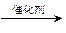 nC6H12O6
nC6H12O6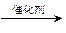 2C2H5OH+2CO2
2C2H5OH+2CO2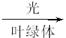 C6H12O6+6O2
C6H12O6+6O2