时间:2021-06-11 05:51:49
1、选择题 下列溶液显酸性的是
A.NaCl溶液
B.Na2CO3溶液
C.AlCl3溶液
D.KNO3溶液
参考答案:C
本题解析:本题考查盐类水解的应用,抓住盐类水解的规律:谁强显谁性,同强显中性,进行相关判断。A、NaCl为强酸强碱盐,不水解,溶液显中性,错误;B、Na2CO3为强碱弱酸盐,碳酸根水解,溶液显碱性,错误;C、AlCl3为强酸弱碱盐,铝离子水解,溶液显酸性,正确;D、KNO3为强酸强碱盐,不水解,溶液显中性,错误。
本题难度:简单
2、选择题 下列各溶液中,物质的量浓度关系正确的是(?)
A.在0.1 mol・L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)
B.常温下,10 mL 0.01 mol・L-1HCl溶液与10 mL 0.01 mol・L-1Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12
C.0.1 mol・L-1的KAl(SO4)2溶液中:c(SO42-)>c(Al3+)>c(OH-)>c(H+)
D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液, 若溶液呈酸性,则有c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-)
若溶液呈酸性,则有c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-)
参考答案:A
本题解析:略
本题难度:一般
3、填空题 某二元酸(化学式用H2B表示)在水中的电离方程式是H2B===H++HB-;HB- H++B2-。回答下列问题。
H++B2-。回答下列问题。
(1)Na2B溶液显_____(填“酸性”、“中性”或“碱性”),理由是_______(用离子方程式表示)。
(2)在0.1 mol・L-1的Na2B溶液中,下列粒子浓度关系式正确的是____。
A.c(B2-)+c(HB-)+c(H2B)=0.1 mol・L-1
B.c(Na+)+c(OH-)=c(H+)+c(HB-)
C.c(Na+)+c(H+)=c(OH-)+c(HB-)+2c(B2-)
D.c(Na+)=2c(B2-)+2c(HB-)
(3)已知0.1 mol・L-1 NaHB溶液的pH=2,则0.1 mol・L-1 H2B溶液中的氢离子的物质的量浓度可能____0.11 mol・L-1(填“<”、“>”或“=”),理由是_____。
(4)0.1 mol・L-1 NaHB溶液中各种离子浓度由大到小的顺序是_______。
参考答案:(1)碱性 B2-+H2O HB-+OH- (2)CD
HB-+OH- (2)CD
(3)< 0.1 mol・L-1NaHB溶液的pH=2,说明其中c(H+)=0.01 mol・L-1,主要是HB-电离产生的,在H2B溶液中,第一步电离产生的H+抑制了第二步的电离,所以0.1 mol・L-1 H2B溶液中c(H+)<0.11 mol・L-1
(4)c(Na+)>c(HB-)>c(H+)>c(B2-)>c(OH-)
本题解析:(1)由H2B===H++HB-(完全电离),HB- H++B2-(部分电离),知Na2B溶液中B2-将发生水解反应,故Na2B溶液显碱性,原因是B2-+H2O
H++B2-(部分电离),知Na2B溶液中B2-将发生水解反应,故Na2B溶液显碱性,原因是B2-+H2O HB-+OH-。
HB-+OH-。
在Na2B溶液中存在:Na2B===2Na++B2-,B2-+H2O HB-+OH-,H2O
HB-+OH-,H2O H++OH-。由电荷守恒知c(Na+)+c(H+)=2c(B2-)+c(OH-)+c(HB-),C对。由物料守恒知c(Na+)=2c(B2-)+2c(HB-)=0.2 mol・L-1,D对。在Na2B溶液中不存在H2B,A错,由物料守恒和电荷守恒知B错。(3)在NaHB溶液中,NaHB===Na++HB-,HB-
H++OH-。由电荷守恒知c(Na+)+c(H+)=2c(B2-)+c(OH-)+c(HB-),C对。由物料守恒知c(Na+)=2c(B2-)+2c(HB-)=0.2 mol・L-1,D对。在Na2B溶液中不存在H2B,A错,由物料守恒和电荷守恒知B错。(3)在NaHB溶液中,NaHB===Na++HB-,HB- H++B2-,H2O
H++B2-,H2O H++OH-。已知0.1 mol
H++OH-。已知0.1 mol
・L-1 NaHB溶液的pH=2,说明其中c(H+)=0.01 mol・L-1,主要是HB-电离产生的。在H2B溶液中,第一步电离产生的H+抑制了第二步的电离,所以0.1 mol・L-1H2B溶液中c(H+)<0.11 mol・L-1。(4)在NaHB溶液中各离子浓度大小顺序为c(Na+)>c(HB-)>c(H+)>c(B2-)>c(OH-)。
本题难度:一般
4、选择题 下列说法中正确的是?(?)
A.常温下,稀释0.1 mol/L的氨水,溶液中c(OH-)、c(NH4+)、c(H+)均下降
B.常温下,c(NH4+)相等的①(NH4)2SO4②(NH4)2Fe(SO4)2③NH4Cl④(NH4)2CO3溶液中,溶质物质的量浓度大小关系是:②<①<④<③
C.pH相等的CH3COONa、NaHCO3和Na2CO3三种溶液:c(CH3COONa)<c(NaHCO3) <c(Na2CO3)
D.某温度时水的离子积常数KW=10-13若将此温度下pH=11的NaOH溶液aL与pH=1的稀硫酸bL混合,若所得混合液PH=2,则a:b=2:9
参考答案:B
本题解析:在稀溶液中c(H+)与c(OH-)的乘积是个定值,不可能同时下降或升高,A项错误;Fe2+的水解抑制NH4+的水解,CO32-的水解促进NH4+的水解,所以等浓度的①(NH4)2SO4、②(NH4)2Fe(SO4)2、③NH4Cl、④(NH4)2CO3溶液c(NH4+)②>①>④>③,因此,c(NH4+)相等的①(NH4)2SO4、②(NH4)2Fe(SO4)2、③NH4Cl、?④(NH4)2CO3溶液中,溶质物质的量浓度大小关系是:②<①<④<③,B项正确;根据越弱越水解可知浓度相同的CH3COONa、NaHCO3和Na2CO3三种溶液的pH为:Na2CO3>NaHCO3>CH3COONa,因此pH相等的CH3COONa、NaHCO3和Na2CO3三种溶液:c(CH3COONa)>c(NaHCO3)>c(Na2CO3),C项错误;pH=11的NaOH溶液c(OH-)=10-2mol/L,pH=1的稀硫酸c(H+)=10-1 mol/L,混合后pH=2则有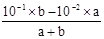 =10-2,则a:b=9:2,D项错误。答案选B。
=10-2,则a:b=9:2,D项错误。答案选B。
点评:本题综合性强,难度大,主要考查学生对知识的分析能力和运用能力。
本题难度:一般
5、选择题 常温条件,下列溶液的有关说法正确的是
A.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
B.0.1 mol/L的NH4Cl溶液中:c(NH4+) = c(Cl-)
C.同为0.1 mol/L的硫酸和氨水等体积混合后:
c(NH4+) + 2c(NH3・H2O) = 2c(SO42-)
D.pH=3的盐酸和pH=11的氨水等体积混合后:c(OH-) = c(H+)
参考答案:A
本题解析:pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,由于醋酸为弱酸,所以醋酸的物质的量远远大于NaOH溶液,所以该混合溶液呈酸性,故滴入石蕊溶液呈红色,所以A正确,为本题的选项;NH4Cl为强酸弱碱盐,所以其水溶液由于水解呈酸性,根据电荷守恒可以知道,c(NH4+) < c(Cl-),故B错误;同为0.1 mol/L的硫酸和氨水等体积混合后,根据物料守恒可以知道c(NH4+) + c(NH3・H2O) = c(SO42-),故C错误;pH=3的盐酸和pH=11的氨水等体积混合,由于一水合氨为弱碱,所以一水合氨的物质的量远远大于HCl的物质的量,故混合后溶液为碱性,所以c(OH-)> c(H+),故D不正确。
点评:本题考查了盐类水解,该知识点是高考考查的重点和难度,本题有一定的综合性,该题难度适中。
本题难度:一般