时间:2021-06-11 05:43:35
1、填空题 科学家一直致力于研究常温、常压下“人工固氮”的新方法。曾有报道:在常温、常压、光照条件下,
N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3和另一种常见气体。进一步研究NH3生成量与温度的关系(其它条件均相同),部分实验数据见下表
回答下列问题:
(1)写出该反应的化学方程式_____________________
(2)该反应的焓变△H______0(填“>”、“<”或“=”)
(3)请在坐标图中画出上述反应在有催化剂与无催化剂两种情况下反应过程中体系能量变化示意图,并进行必要标注。
(4)与目前广泛使用的工业合成氨方法相比,该方法中固氮反应速率慢。请提出可提高其反应速率且增大NH3生成量的建议:___________________。
(5)已知:
N2(g) + 3H2(g) == 2NH3(g) △H = -92.4 kJ/mol
H2(g) + Cl2(g) == 2HCl(g) △H = -184.6 kJ/mol?
1/2N2(g) + 2H2(g) + 1/2Cl2(g) == NH4Cl(s) △H = -313.6 kJ/mol
① 计算NH3(g) + HCl(g) == NH4Cl(s)的反应焓变:△H =______________
② 室温下NH3就和HCl能发生化合反应生成NH4Cl;而在加热的条件下,NH4Cl则能分解为NH3和HCl。请用所学的化学原理解释这一现象:____________________________
参考答案:(1)2N2 + 6H2O == 4NH3 + 3O2
(2)> (3)“略”
(4)升高温度,增大反应物N2的浓度(并不断移出生成物脱离反应体系)
(5)① -175.1 kJ/mol;② NH3(g) + HCl(g) == NH4Cl(s)是一个焓减、熵减的反应,在低温下自发,在高温(加热条件)下不自发。而其逆反应NH4Cl的分解则在高温下自发
本题解析:
本题难度:一般
2、填空题 “西气东输”工程使北京用上了更加清洁的能源--天然气(主要成分是CH4)。在使用天然气以前北京用的煤气主要是将碳与水蒸气在高温下反应制得的水煤气,水煤气的主要成分是CO和H2,两者的体积比约为
1:1。 已知:CO的燃烧热△H=-283.0 kJ/mol;H2的燃烧热△H=-286.0 kJ/mol;CH4的燃烧热△H=-890.0 kJ/mol。
(1)用H2为原料设计成氢氧燃料电池(电解质溶液为KOH),正极的电极反应式是:_______________。
(2)已知: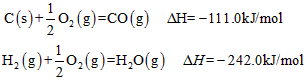
写出由C(s)与H2O(g)反应生成水煤气的热化学方程式:______________________。
(3)忽略水煤气中其它成分,若获得相等的热量,所需相同状况下水煤气与甲烷的体积比约为_______;排放的CO2物质的量的比约为_________。通过计算得知:使用天然气能______(填“增多”或“减少”)温室气体(CO2)的排放。(各种燃料均完全燃烧)
(4)若将由amolCH4、CO和H2组成的混合气体完全燃烧,生成CO2气体和液态水时放出热量(Q)的取值范围是___________。
参考答案:(1)
(2)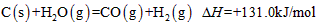 (3)3:1;3:2 ;减少
(3)3:1;3:2 ;减少
(4)890.0a kJ>Q>283.0a kJ
本题解析:
本题难度:一般
3、填空题 二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物。综合治理其污染是环境化学当前的重要研究内容之一。
(1)硫酸生产中,SO2催化氧化生成SO3: 2SO2(g)+O2(g) 2SO3(g) 某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如图所示。
2SO3(g) 某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如图所示。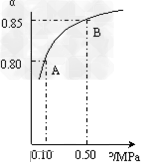
根据图示回答下列问题:
①将2.0mol?SO2和1.0mol?O2置于10L密闭容器中,反应达平衡后,体系总压强为0.10MPa。该反应的平衡常数表达式为:__________;等于____________。
②平衡状态由A变到B时.平衡常数K(A)_______K(B)(填“>”、“<”或“=”)。
(2)用CH4催化还原NOx可以消除氮氧化物的污染。
例如:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)?△H=-574?kJ・mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)?△H=-1160?kJ・mol-1
若用标准状况下4.48L?CH4还原NO2至N2整个过程中转移的电子总数为______(阿伏加德罗常数的值用NA表示),放出的热量为______kJ。
(3)新型纳米材料氧缺位铁酸盐(MFe2Ox?3<x<4,M=Mn、Co、Zn或Ni)由铁酸盐(MFe2O4)经高温还原而得,常温下,它能使工业废气中的酸性氧化物分解除去。转化流程如图所示: 请写出MFe2Ox分解SO2的化学方程式___________(不必配平)。 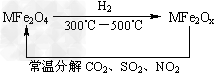
参考答案:(1)①k=c2(SO3)/c(O2) c2(SO2) ;?800 L・mol-1?;② =
(2)1.60NA(或1.6NA) ;173.4。
(3)MFe2Ox+SO2 MFe2O4+S
MFe2O4+S
本题解析:
本题难度:一般
4、选择题 在298K、100kPa时,已知:2H2O(g) = 2H2(g) + O2(g) ΔH1; Cl2(g) + H2(g) = 2HCl(g) ΔH2
2Cl2(g) + 2H2O(g) = 4HCl(g) + O2(g) ΔH3; 则ΔH3与ΔH1和ΔH2间的关系正确的是
[? ]
A.ΔH3=ΔH1+2ΔH2
B.ΔH3=ΔH1+ΔH2
C.ΔH3=ΔH1-2ΔH2
D.ΔH3=ΔH1-ΔH2
参考答案:A
本题解析:
本题难度:一般
5、填空题 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的ΔH表示生成
1 mol产物的数据)。
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式是_____________________。
(2)PCl5分解成PCl3和Cl2的热化学方程式是__________________________。
(3)工业上制备PCl5通常分两步进行,先将P和Cl2反应生成中间产物PCl3,然后降温,再和Cl2反应生成
PCl5。原因是___________________。
(4)P和Cl2分两步反应生成1 mol PCl5的ΔH3=__________,P和Cl2一步反应生成1 mol PCl5的ΔH4________ΔH3(填“大于”“小于”或“等于”)。
参考答案:(1)3/2Cl2(g)+P(s)==PCl3(g) ΔH=-306 kJ/mol
(2)PCl5(g)==PCl3(g)+Cl2(g) ΔH=+93 kJ/mol
(3)两步反应均为放热反应,降温有利于提高产率,防止生成物分解
(4)-399kJ/mol;等于
本题解析:
本题难度:一般