时间:2021-06-11 05:42:09
1、选择题 常温下,0.1mol/L某一元酸(HA)的pH>1,在0.1mol/L某一元碱(BOH)中H+和OH—离子物质的量浓度的关系为: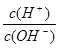 ?=10-12,将这两种溶液等体积混合,所得溶液各离子物质的量浓度关系不正确的是(? )
?=10-12,将这两种溶液等体积混合,所得溶液各离子物质的量浓度关系不正确的是(? )
A. C(B+)>C(A-)>C(OH-)>C(H+)
B. C(A-)>C(B+)>C(H+)>C(OH-)
C. C(B+)=C(A-) + C(HA)?
D. C(B+)+ C(H+)=C(A-)+ C(OH-)
参考答案:B
本题解析:常温下,0.1mol/L某一元酸(HA)的pH>1,所以HA是弱酸。又因为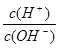 =10-12,所以根据水的离子积常数可知,溶液中OH-物质的量浓度是0.1mol/L,这说明BOH是一元强碱。二者混合后恰好反应,生成强碱弱酸盐,水解显碱性,因此A、D正确,B不正确。C符合物料守恒,正确,答案选B。
=10-12,所以根据水的离子积常数可知,溶液中OH-物质的量浓度是0.1mol/L,这说明BOH是一元强碱。二者混合后恰好反应,生成强碱弱酸盐,水解显碱性,因此A、D正确,B不正确。C符合物料守恒,正确,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题,试题贴近高考,基础性强,侧重考查学生分析问题、解决问题的能力。该题的关键是准确判断出酸碱的强弱,然后灵活运用即可。
本题难度:简单
2、填空题 (4分)科学家预言, 将成为21世纪替代矿物燃料的理想能源,该能源有三个主要优点:(1) ;(2) ;(3) 。
参考答案:(每空1分,共4分)
氢气 (1)来源丰富 (2)单位质量放热多 (3)生成物无污染
本题解析:氢气将成为21世纪替代矿物燃料的理想能源。
该能源有三个主要优点:(1) 来源丰富 (2)单位质量放热多 (3)生成物无污染
本题难度:简单
3、选择题 等体积等浓度的MOH强碱溶液和HA弱酸溶液混和后,混和液中有关离子的浓度应满足的关系是
A.c(M+)>c( OH―)> c(A-)>c(H+)
B.c(M+)> c(A-)>c(H+)>c( OH―)
C.c(M+)> c(A-)>c( OH―)>c(H+)
D.c(M+)>c(H+) ="c(" OH―)+ c(A-)
参考答案:C
本题解析:略
本题难度:简单
4、选择题 常温下下列四种溶液,由水电离生成的H+的物质的量浓度之比为(?)
①pH=0的盐酸?②0.1 mol·L-1的盐酸?③0.01 mol·L-1的NAOH溶液?④pH=11的NAOH溶液
A.1∶10∶100∶1000
B.0∶1∶12∶11
C.14∶13∶12∶11
D.14∶13∶2∶1
参考答案:A
本题解析:①中,c(H+)="1" mol·L-1,c(OH-)= (H+)=10-14 mol·L-1
(H+)=10-14 mol·L-1
②中,c(H+)="0.1" mol·L-1,c(OH-)= (H+)=10-13 mol·L-1
(H+)=10-13 mol·L-1
③中,c(OH-)=10-2 mol·L-1, (H+)=10-12 mol·L-1
(H+)=10-12 mol·L-1
④中,pOH=3,c(OH-)=10-3 mol·L-1, (H+)=10-11 mol·L-1。
(H+)=10-11 mol·L-1。
本题难度:简单
5、选择题 100 mL pH=2的两种一元酸x和y,稀释过程中pH与溶液体积的关系如图所示。下列说法正确的是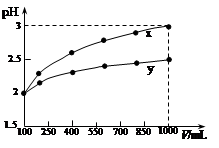
A.稀释前x、y的物质的量浓度相等
B.x为强酸,y为弱酸
C.随着稀释的进行,y的电离程度减小
D.等体积的x、y分别分别与足量的锌反应,x放出的氢气多
参考答案:B
本题解析:根据图像可知,稀释10倍,X的pH从2变为3,所以X是强酸,但Y的pH从2变为2.5,这说明在稀释过程中,有氢离子电离出来,所以Y是弱电解质,因此B正确。A不正确,稀释前Y的浓度大,C不正确,稀释促进电离。D不正确,应该是是Y发出的氢气多,答案选B。
本题难度:简单