时间:2021-06-11 05:41:01
1、填空题 在T1℃时,向容积为2 L的密闭容器甲中加入1molA 气体、3mol B气体及少量固体催化剂,发生下列反应:A(g)+3B(g)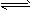 2C(g);△H
2C(g);△H 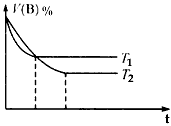
(1)计算该反应在0~10 min时间内B的平均反应速率为________,A的转化率为_______
(2)在T1℃时,若起始在容器甲中只加入1.0 molC,则达到平衡时C的体积分数____。
a.大于25% b.等于25% c.小于25%
(3)上图分别表示的是在T1℃和T2℃时,密闭容器甲中气体B的体积分数随时间(t)变化的曲线,试判断T1 ____(填“<”“>”或“=”)T2。
(4)若保持T1℃,在体积也为2L的密闭容器乙中通入一定量的A、B、C三种气体,欲使平衡时容器乙中各物质的物质的量与容器甲中完全相同,且起始时反应向正反应方向进行,则通入B的物质的量x的取值范围是_____________________
2、选择题 对于反应2A(气)+xB(气)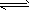 4C(气)达到平衡时,C的浓度为1.2mol/L,当其它条件不变,把体积扩大1倍时,测得C的浓度为0.7mol/L,则x的值为
4C(气)达到平衡时,C的浓度为1.2mol/L,当其它条件不变,把体积扩大1倍时,测得C的浓度为0.7mol/L,则x的值为
[? ]
A.1
B.2
C.3
D.4
3、填空题 A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的气球。关闭K2,将等量且少量的NO2通过K1、K3分别充人A、B中,反应起始时,A、B的体积相同。(已知:2NO2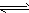 N2O4;△H<0) (如下图)
N2O4;△H<0) (如下图)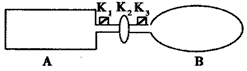
(1)一段时间后,反应达到平衡,此时A、B中生成的N2O4的速率是VA_________VB。(填“>”.“<”.“=”);若打开活塞K2,气球B将__________(填:变大、变小、不变)。
(2)若在A、B中再充人与初始量相等的NO2,则达到平衡时,NO2的转化率αA将_________ (填增大或减小.不变);若通人等量的Ne气,则达到平衡时,A中NO2的转化率将_________,B中NO2的转化率将_________(填: 变大、变小、不变)。
(3)室温下,若A、B都保持体积不变,将A套上一个绝热层,B与外界可以进行热传递,则达到平衡时,_________中的颜色较深。
(4)若在容器A中充人4.6g的NO2,达到平衡后容器内混合气体的平均相对分子质量为57.5,则平衡时N2O4的物质的量为_________
4、选择题 在温度不变下,在恒压容器a与恒容容器b中,分别充入体积比为1:3的N2和H2.若开始时两容器的体积相等,且在相同条件下达到平衡时,两容器中N2的转化率应当是( )
A.a中大
B.b中大
C.a、b一样大
D.无法判断
5、选择题 对于平衡体系mA(g)+nB(g)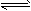 pC(g)+qD(g);△H<0 。下列结论中不正确的是
pC(g)+qD(g);△H<0 。下列结论中不正确的是
[? ]
A.若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则m+n<p+q
B.若平衡时,A、B 的转化率相等,说明反应开始时,A、B的物质的量之比为 m : n
C.若温度不变时,压强增大到原来的2倍,达到新平衡时,总体积一定比原来的1/2要小
D.若m+n=p+q,则往含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a mol