时间:2021-02-18 07:28:44
1、填空题 Ⅰ、向Cu、Cu2O和CuO组成的混合物中,加入1 L 0.6 mol・L -1HNO3溶液恰好使混合物溶解,同时收集到2240 mL NO气体(标准状况)。(已知:Cu2O+2H+=Cu+Cu2++H2O)
(1)Cu2O跟稀硝酸反应的离子方程式 。
(2)若将上述混合物用足量的H2加热还原,所得到固体的质量为 g。
(3)若混合物中含0.1 mol Cu,将该混合物与稀硫酸充分反应,至少消耗H2SO4的物质的量为 。
Ⅱ、一定温度下,向一容积为5 L的恒容密闭容器中充入0.4 mol SO2和0.2 mol O2,发生反应:2SO2(g)+O2(g)  2SO3(g)。当反应达到平衡时,容器内压强变为起始时的0.7倍。
2SO3(g)。当反应达到平衡时,容器内压强变为起始时的0.7倍。
请回答下列问题:
(4)判断该反应达到化学平衡状态的标志是 (填字母)。
A.SO2、O2、SO3三者的浓度之比为2∶1∶2
B.容器内气体的压强不变
C.容器内混合气体的密度保持不变
D.SO3的物质的量不再变化
E.SO2的生成速率和SO3的生成速率相等
(5) SO2的转化率 。
2、选择题 (NH4)2Cr2O7是一种受热易分解的盐。下列各组对(NH4)2Cr2O7受热分解产物的判断,符合实际的是
A.CrO3 + NH3 + H2O
B.Cr2O3 + NH3 + H2O
C.CrO3 + N2 + H2O
D.Cr2O3 + N2+ H2O
3、选择题 下列结构示意图中,表示阴离子的是
A.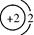
B.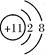
C.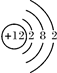
D.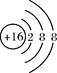
4、选择题 在铜的催化作用下氨气与氟气反应,得到一种三角锥形分子M和一种铵盐N。下列有关说法错误的是
A.该反应的化学方程式为4NH3+3F2→ NF3+3NH4F
B.M是极性分子,其还原性比NH3强
C.M既是氧化产物,又是还原产物
D.N中既含有离子键,又含有共价键
5、选择题 化学用语是学习化学的重要工具。以下化学用语表示错误的是
A.质量数之和是质子数之和两倍的水分子符号可能是:
B.NaHCO3水溶液呈碱性的原因:
C.基态硫离子的电子排布式:
D.熔融状态下硫酸氢钠的电离方程式: (熔融)=
(熔融)=