时间:2021-02-18 07:24:06
1、选择题 设NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.1 mol氦气中有2NA个氦原子
B.14 g氮气中含NA个氮原子
C.2 L 0.3 mol·L-1 Na2SO4溶液中含0.6 NA个Na+
D.18 g水中所含的电子数为8NA
参考答案:B
本题解析:A.氦气是单原子分子,所以1 mol氦气中有NA个氦原子,错误;B.N原子相对原子质量是14,所以14 g氮气中含NA个氮原子,正确;C.2 L 0.3 mol·L-1 Na2SO4溶液中含1.2 NA个Na+ ,错误;D.18 g水的物质的量是1mol,由于水分子中含有10个电子,因此18g的水中所含的电子数为10NA,错误。
考点:考查阿伏加德罗常数的计算的知识。
本题难度:一般
2、选择题 1 mol Na2O2与2 mol NaHCO3固体混合后,在密闭的容器中加热充分反应,排出气体物质后冷却,残留的固体物质是(?)
A.Na2CO3
B.Na2O2、Na2CO3
C.NaOH、Na2CO3
D.Na2O2、NaOH、Na2CO3
参考答案:A
本题解析:由题可知,该过程发生的反应为:2NaHCO3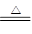 Na2CO3+H2O+CO2↑,
Na2CO3+H2O+CO2↑,
2Na2O2+2CO2=2Na2CO3+O2↑,2Na2O2+2H2O=4NaOH+O2↑,2 mol NaHCO3固体反应生成了1mol水和1mol二氧化碳,所以而生成的二氧化碳刚好与过氧化钠反应,而不与水反应,因为水加热被蒸发了,所以残留的固体物质是Na2CO3 ,故本题的答案选择A。
点评:本题考查了钠及其化合物,该知识点是高考考查的重点和难度,本题比较抽象,有一定的难度。
本题难度:一般
3、选择题 某实验室用下列溶质配制一种混合溶液,已知溶液中c(K+)=c(Cl-)=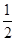 c(Na+)=c(SO42-)(c表示物质的量浓度),则其溶质可能是
c(Na+)=c(SO42-)(c表示物质的量浓度),则其溶质可能是
A.KCl、Na2SO4
B.KCl、Na2SO4、NaCl
C.NaCl、Na2SO4、K2SO4
D.KCl、K2SO4、Na2SO4
参考答案:AC
本题解析:A、若KCl、Na2SO4的物质的量相同时,则电离生成的离子关系为 c(K+)=c(Cl-)=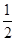 c(Na+)=c(SO42-),故A正确;B、若c(K+)=c(Cl-),则该溶液中溶质不可能有氯化钠,故B错误;C、若c(K+)=c(Cl-),则硫酸钾的物质的量是氯化钠的2倍。则只要在满足硫酸钠的物质的量等于硫酸钾即可满足c(K+)=c(Cl-)=
c(Na+)=c(SO42-),故A正确;B、若c(K+)=c(Cl-),则该溶液中溶质不可能有氯化钠,故B错误;C、若c(K+)=c(Cl-),则硫酸钾的物质的量是氯化钠的2倍。则只要在满足硫酸钠的物质的量等于硫酸钾即可满足c(K+)=c(Cl-)=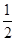 c(Na+)=c(SO42-)成立,故C正确;D、KCl、K2SO4、无论以何种比例混合,都c(K+)>c(Cl-),因此不会满足C c(K+)=c(Cl-)=
c(Na+)=c(SO42-)成立,故C正确;D、KCl、K2SO4、无论以何种比例混合,都c(K+)>c(Cl-),因此不会满足C c(K+)=c(Cl-)=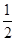 c(Na+)=c(SO42-),故D错误,答案选AC。
c(Na+)=c(SO42-),故D错误,答案选AC。
本题难度:一般
4、选择题 某溶液中大量存在以下五种离子:NO3-、SO42-、Fe3+、H+、M,其物质的量之比为n(NO3-)∶n(SO42-)∶n(Fe3+)∶n(H+)∶n(M)=2∶3∶1∶3∶1, 则 M可能为
A.Fe2+
B.Mg2+
C.CO32-
D.Ba2+
参考答案:B
本题解析:
由物质的量之比为n(NO3-):n(SO42-):n(Fe3+):n(H+):n(M)=2:3:1:3:1,根据溶液的电中性原则,则阴离子所带的负电荷总数等于阳离子所带的正电荷总数,而负电荷数为2×1+3×2>正电荷数1×3+3×1,则M为阳离子,由电荷守恒可知,M为带两个单位正电荷的阳离子,又Fe2+、NO3-、H+发生氧化还原反应,则M一定为Mg2+,答案选B。
考点:考查电荷守恒的应用
点评:本题考查了电荷守恒的应用,溶液的电中性,难度不大。需要从阴阳离子所带的电荷数上分析,由溶液的电中性为依据,还要注意Fe2+与题干中的离子不共存这一特殊性质。
本题难度:一般
5、选择题 冬季的降雪给机场和马路带来诸多不便,其中醋酸钾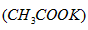 是融雪效果较好的融雪剂,下列关于醋酸钾说法正确的是
是融雪效果较好的融雪剂,下列关于醋酸钾说法正确的是
[? ]
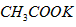 质量为98
质量为98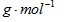
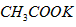 的摩尔质量等于它的相对分子质量
的摩尔质量等于它的相对分子质量 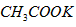 质量约为
质量约为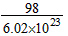 g
g 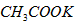 的物质的量为1 mol?
的物质的量为1 mol? 参考答案:C
本题解析:
本题难度:一般