±º‰:2021-02-18 07:22:01
1°¢—°‘Ò ‘⁄ºÓ–‘Ãıº˛œ¬ƒÐπª¥Û¡øπ≤¥Ê£¨∂¯‘⁄«øÀ·–‘Ãıº˛œ¬»¥ƒÐ∑¢…˙—ıªØªπ‘≠∑¥”¶µƒ¿Î◊”◊È «(? )
A£Æ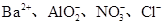
B£ÆK+°¢Na+°¢ClO-°¢Fe2+
C£Æ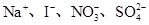
D£Æ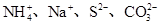
2°¢—°‘Ò ‘⁄ºÓ–‘»Ð“∫÷–ƒÐ¥Û¡øπ≤¥Ê£¨≤¢«“»Ð“∫Œ™ŒÞ…´Õ∏√˜µƒ «£®°°°°£©
A£ÆNa+°¢K+°¢MnO4-°¢SO42-
B£ÆNH4+°¢Na+°¢NO3-°¢Cl-
C£ÆK+°¢Ba2+°¢NO3-°¢Cl-
D £ÆMg2+°¢Fe3+°¢Cl-°¢NO3-
3°¢—°‘Ò œ¬¡–∏˜◊È÷–µƒ¿Î◊”£¨ƒÐ‘⁄»Ð“∫÷–¥Û¡øπ≤¥Êµƒ «
[? ]
A£ÆMg2+°¢H+°¢C1-°¢OH-°°°°°°°°
B£ÆK+°¢Cu2+°¢NO3-°¢SO42-
C£ÆNa+°¢OH-°¢Cl-°¢CO32-°° °°°°
D£ÆNa+°¢Ba2+°¢CO32-°¢NO3-
4°¢ÃÓø’ œ÷”–ŒÂ÷÷ø…»Ð–‘ŒÔ÷ A°¢B°¢C°¢D°¢E£¨À¸√«À˘∫¨“ı°¢—Ù¿Î◊”ª•≤ªœýÕ¨£¨∑÷±∫¨”–ŒÂ÷÷—Ù¿Î◊”Na£´°¢Al3£´°¢Mg2£´°¢Ba2£´°¢Fe3£´∫ÕŒÂ÷÷“ı¿Î◊”Cl£≠°¢OH£≠°¢NO3°™°¢CO32°™µƒ“ª÷÷°£
(1)ƒ≥Õ¨—ßÕ®π˝±»Ωœ∑÷Œˆ£¨»œŒ™ŒÞ–˺ϗÈæÕø…≈–∂œ∆‰÷–±ÿ”–µƒ¡Ω÷÷ŒÔ÷ «________∫Õ________(Ãѧ Ω)°£
(2)Œ™¡À»∑∂®X£¨œ÷Ω´(1)÷–µƒ¡Ω÷÷ŒÔ÷ º«Œ™A∫ÕB£¨∫¨XµƒŒÔ÷ º«Œ™C£¨µ±C”ÎBµƒ»Ð“∫ªÏ∫œ ±£¨≤˙…˙∫Ï∫÷…´≥¡µÌ∫Ռޅ´ŒÞŒ∂∆¯Ã£ªµ±C”ÎAµƒ»Ð“∫ªÏ∫œ ±≤˙…˙◊ÿª∆…´≥¡µÌ£¨œÚ∏√≥¡µÌ÷–µŒ»Îœ°œıÀ·≥¡µÌ≤ø∑÷»ÐΩ‚£¨◊Ó∫Û¡Ù”–∞◊…´≥¡µÌ≤ª‘Ÿ»ÐΩ‚°£‘ÚXŒ™________°£
A£ÆSO32°™? B£ÆSO4°™ C£ÆCH3COO£≠? D£ÆSiO32°™
(3)Ω´CuÕ∂»ÎµΩ◊∞”–D»Ð“∫µƒ ‘πÐ÷–£¨Cu≤ª»ÐΩ‚£ª‘ŸµŒº”œ°H2SO4£¨Cu÷Ω•»ÐΩ‚£¨πÐø⁄∏ΩΩ¸”–∫Ï◊ÿ…´∆¯ÃÂ≥ˆœ÷°£‘ÚŒÔ÷ D“ª∂®∫¨”–…œ ˆ¿Î◊”÷–µƒ________ (ÃÓœý”¶µƒ¿Î◊”∑˚∫≈)°£”–πÿ∑¥”¶µƒ¿Î◊”∑Ω≥Ã ΩŒ™_____________________________________°£
(4)¿˚”√…œ ˆ“—æ≠»∑∂®µƒŒÔ÷ £¨ø…“‘ºÏ—È≥ˆD°¢E÷–µƒ—Ù¿Î◊”°£«ÎºÚ ˆ µ—È≤Ÿ◊˜≤Ω÷Ë°¢œ÷œÛº∞Ω·¬€£∫______________________________________________
5°¢—°‘Ò ‘⁄ÀƵÁ¿Î≥ˆµƒC(H+)=10-14mol/Lµƒ»Ð“∫÷–£¨“ª∂®ƒÐ¥Û¡øπ≤¥Êµƒ¿Î◊”◊È «?£®?£©
A£ÆK+°¢Na+°¢HCO3-°¢Cl-
B£ÆK+°¢AlO2-°¢Br-°¢Cl-
C£ÆNa+°¢Cl-°¢NO3-°¢SO42-
D£ÆAl3+°¢NH4+°¢Cl-°¢SO42-