时间:2021-02-18 07:19:10
1、选择题 在2A + B = 3C + 4D的反应中,下列表示该反应速率最大的是
[? ]
A. (A)=0.5 mol・L-1・min-1
(A)=0.5 mol・L-1・min-1
B. (B)=0.3 mol・L-1・min-1
(B)=0.3 mol・L-1・min-1
C. (A)=0.8 mol・L-1・min-1
(A)=0.8 mol・L-1・min-1
D. (D)=1 mol・L-1・min-1
(D)=1 mol・L-1・min-1
2、选择题 对于反应:N2+3H2 2NH3(正反应为放热反应),下列图象所示不正确的是(?)
2NH3(正反应为放热反应),下列图象所示不正确的是(?)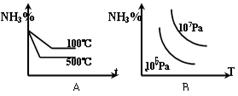
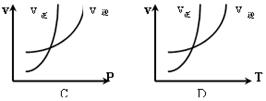
w.k.
3、填空题 如图所示,当关闭K时,向A中充入4molX、14molY,向B中充入2molX、7molY,起始时V(A)=V(B)=a升,在相同温度和有催化剂存在的条件下,两容器各自发生下列反应:2X(g)+2Y(g) Z(g)+2W(g) △H<0。达到平衡(Ⅰ)时,B中密度变为原来的
Z(g)+2W(g) △H<0。达到平衡(Ⅰ)时,B中密度变为原来的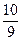 ,试回答:
,试回答: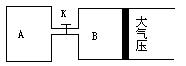
(1)设A、B两容器中化学平衡常数分别为K1和K2,则它们的大小关系是K1____K2(填“大于”或“等于”或“小于”)。
(2)B中X的转化率α(X)B为?。
(3)A中Z和B中的W物质的量的比较:
n(Z)A?n(W)B(填“大于”或“等于”或“小于”)。
(4)打开K,过一段时间重新达平衡(Ⅱ)时,B的体积为?升(用含a的代数式表示,连通管中气体体积不计);在温度不变的情况下,要使B容器恢复原来反应前的体积,可采取的措施是?。
4、填空题 (12分)
(1)在密闭容器里,通入x mol SO2和y mol O2,发生化学反应:2SO2 (g) + O2 (g) 2SO3 (g) ;当其它条件不变时,改变下列条件,反应速率将如何改变?(填“增大”“减小”或“不变”)
2SO3 (g) ;当其它条件不变时,改变下列条件,反应速率将如何改变?(填“增大”“减小”或“不变”)
①降低温度____________________ ;?
②当容器容积不变,充入更多的O2 ____________________ ;?
③当容器容积不变,通入氖气____________________。
(2)来自石油的基本化工原料苯和乙烯,都有着十分广泛的用途。请回答:
④可以用来鉴别苯蒸气和乙烯的试剂是____________________(填序号)。
A.水? B.溴的四氯化碳溶液? C.酸性高锰酸钾溶液
⑤苯分子具有平面正六边形结构,所有原子共一个平面,则苯分子中在一条直线上的原子最多有____________________ 个。
⑥在一定条件下,乙烯能与水发生加成反应生成有机物A,写出A与Na反应的化学方程式________________________________________。
5、选择题 下列图示与对应的叙述相符的是 ?
? ?
? ?
?
甲?乙?丙?丁
A.图甲可以判断出反应A(g) + B(g) 2C(g) 的△H<0,T2>T1
2C(g) 的△H<0,T2>T1
B.图乙表示压强对可逆反应2A(g) + 2B(g) 3C(g) + D(s)的影响,乙的压强比甲的压强大
3C(g) + D(s)的影响,乙的压强比甲的压强大
C.据图丙,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH≈4
D.图丁表示25℃时,用0.1 mol・L―1盐酸滴定20 mL 0.1 mol・L-1 NaOH溶液,溶液的pH随加入盐酸体积的变化