ʱ��:2021-02-18 07:15:37
1��ѡ���� �������ӷ���ʽH++OH-=H2O��ʾ�Ļ�ѧ��Ӧ�ǣ�������
A��CH3COOH+NaOH=CH2COONa+H2O
B��2HNO3+Mg��OH��=Mg��NO3��2+2H2O
C��H2SO4+Ba2��OH��2=BaSO4��+2H2O
D��2HCl+Ba��OH��2=BaCl2+2H2O
�ο��𰸣�A��CH3COOH+NaOH=CH2COONa+H2O�����ӷ�ӦΪCH3COOH+OH-=CH2COO-+H2O����A��ѡ��
B��2HNO3+Mg��OH��=Mg��NO3��2+2H2O�����ӷ�ӦΪ2H++Mg��OH��=Mg2++2H2O����B��ѡ��
C��H2SO4+Ba2��OH��2=BaSO4��+2H2O�����ӷ�ӦΪ2H++SO42-+Ba2++2OH-=BaSO4��+2H2O����C��ѡ��
D��2HCl+Ba��OH��2=BaCl2+2H2O�����ӷ�ӦΪH++OH-=H2O����Dѡ��
��ѡD��
���������
�����Ѷȣ���
2��ѡ���� ������������ȷ����
A��0.1mol/L��Na2S��Һ�У�c(OH-)=c(H+)+c(HS-)+2c(H2S)
B��0.1mol/LNa2CO3��Һ�У�c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)]
C��Ũ�Ⱦ�Ϊ0.1mol/L��̼������Һ�Ͱ�ˮ��Һ�У���ˮ�������c(OH-)��ǰ�ߴ��ں���
D��0.1mol/LNH4Cl��0.1mol/L NH3��H2O����������Һ��pH>7����c(NH4+)>c(Cl-)>c(OH-)>c(NH3��H2O)>c(H+)
�ο��𰸣�D
���������A������ȷ��Na2S��Һʹ��̪��Һ��죺S2����H2O 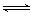 OH����HS�D
OH����HS�D
B������ȷ���ڴ�����Һ�м���Na2CO3��Һ��CO32����2CH3COOH��CO2����H2O2CH3COO�D
C������ȷ��NH4HCO3��Һ�����NaOH��Һ��ϣ�NH4+��HCO3�D��2OH����NH3?H2O��CO32�D��H2O
D����ȷ��
�����Ѷȣ�һ��
3��ѡ���� ����ȷ��ʾ���з�Ӧ�����ӷ���ʽΪ
A��̼��������Һ�е�������������Һ��HCO3����OH��=CO32����H2O
B����������ͨ�����������Һ��SO2��ClO����2OH��=SO42����Cl����H2O
C��������ϡ���BaS��2H��=H2S����Ba2��
D����ǿ����Һ�д���������Fe(OH)3��Ӧ����Na2FeO4��3ClO����2Fe(OH)3=2FeO42����3Cl����H2O��4H��
�ο��𰸣�B
���������ѡ��A��NaHCO3��Һ��Ca(OH)2��Һ��Ӧһ������CaCO3��ѡ��B������Һ��ClO���ܽ�SO2����ΪSO42����ѡ��C��BaS��ϡ���ᷴӦ���ɸ����ܵ�BaSO4������ѡ��D����ǿ����Һ�У�����������H����
�����Ѷȣ�һ��
4������� ��1��Mg��OH��2�л��е�Al��OH��3�����ʿ�����NaOH��ȥ���������ӷ���ʽ��ʾ______
��2��Fe3+�ļ��������ӷ���ʽ��ʾ______
��3������������������Һʱ�������������ۣ���˵��ԭ��______�������ӷ���ʽ��ʾ��
��4������ˮ��Һ��______�ԣ����ᡢ��У���ԭ��______�������ӷ���ʽ��ʾ��
��5��д��þ���ڶ�����̼��ȼ�յĻ�ѧ����ʽ______��
�ο��𰸣���1���������������ܽ���NaOH��Һ�У���������þ���ܣ�Mg��OH��2�л��е�Al��OH��3�����ʿ�����NaOH��ȥ�����ӷ�ӦΪAl��OH��3+OH-=AlO2-+2H2O��
�ʴ�Ϊ��Al��OH��3+OH-=AlO2-+2H2O��
��2������KSCN��Һ���������ӣ���ҺΪѪ��ɫ�����ӷ�ӦΪFe3++3SCN- Fe��SCN��3����Ӧ���ɺ��ɫ���������ӷ�ӦΪFe3++3OH-=Fe��OH��3��
Fe��SCN��3����Ӧ���ɺ��ɫ���������ӷ�ӦΪFe3++3OH-=Fe��OH��3��
�ʴ�Ϊ��Fe3++3SCN- Fe��SCN��3��Fe3++3OH-=Fe��OH��3��
Fe��SCN��3��Fe3++3OH-=Fe��OH��3��
��3����������������Һʱ�������������ۣ��������������ױ������������������2Fe3++Fe=3Fe2+���ʴ�Ϊ��2Fe3++Fe=3Fe2+����������������������������������������������
��4������ˮ��Һ����������ˮ��ʹ��Һ�Լ��ԣ����������ӷ�ӦΪS2-+H2O HS-+OH-���ʴ�Ϊ�����ԣ�S2-+H2O
HS-+OH-���ʴ�Ϊ�����ԣ�S2-+H2O HS-+OH-��������������������
HS-+OH-��������������������
��5��Mg�ڶ�����̼��ȼ����������þ��̼�������Ļ�ѧ��ӦΪ2Mg+CO2��ȼ.2MgO+C���ʴ�Ϊ��2Mg+CO2��ȼ.2MgO+C��
���������
�����Ѷȣ�һ��
5��ѡ���� �������ӷ���ʽ��д��ȷ���ǣ�?��
A����������ͭ��Һ��Ӧ��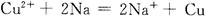
B��м���ڹ���ϡ���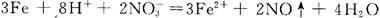
C��ʯ��ʯ���ڴ��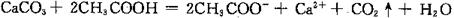
D��FeI2��Һ��ͨ������������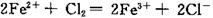
�ο��𰸣�C
������������ǻ��õĽ���������ˮ��Ӧ������Һ�к�����ͭ��Ӧ�ò���ͭ���ʣ�A����ȷ��B�������ǹ����ģ�Ӧ��������������B����ȷ�������ӵĻ�ԭ��ǿ���������ӵģ��������������������ǵ����ӣ�D����ȷ����ѡC��
���������ж����ӷ���ʽ��ȷ���ķ���һ���ǣ���1����鷴Ӧ�ܷ�������2����鷴Ӧ��������Ƿ���ȷ����3���������ʲ���Ƿ���ȷ����4������Ƿ�����غ��ϵ���磺�����غ�͵���غ�ȣ�����5������Ƿ����ԭ��ѧ����ʽ��
�����Ѷȣ�һ��