时间:2021-02-18 07:07:06
1、选择题 含SO2的烟气会形成酸雨,工业上常利用Na2SO3溶液作为吸收液脱除烟气中的SO2。随着SO2的吸收,吸收液的pH不断变化。下列粒子浓度关系一定正确的是:
A.Na2SO3溶液中存在: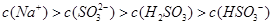
B.已知NaHSO3溶液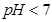 ,该溶液中:
,该溶液中: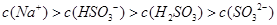
C.当吸收液呈中性时: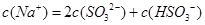
D.当吸收液呈酸性时: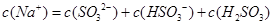
2、选择题 在溶液中能大量共存的一组离子或分子是( )
A.NH4+、H+、NO3-、HCO3-
B.K+、Al3+、SO42-、NH3?H2O
C.Na+、K+、SO32-、Cl2
D.Na+、CH3COO-、CO32-、OH-
3、选择题 下列离子组能在酸性溶液中大量共存的是?
A.K+、Mg2+、Cl-、SO32-
B.Cu2+、K+、Cl-、SO42-
C.NH4+、Na+、CO32-、OH-
D.Ca2+、HSO3-、K+、SO42-
4、选择题 在碱性溶液中能大量共存且为无色透明的溶液是( )
A.K+、Cl-、MnO4-、SO42-
B.Na+、Cu2+、NO3-、CO32-
C.Na+、NO3-、SO42-、HCO3-
D.Na+、SO42-、Cl-、NO3-
5、选择题 若溶液中由水电离的c(OH-)=1×10-14mol/L,则在此溶液中一定不能大量共存的离子组是( )
A.Al3+?Na+NO3-Cl-
B.K+Na+Cl-NO3-
C.K+Na+SO32-NO3-
D.K+NH4+SO42-HCO3