时间:2021-02-18 06:46:58
1、选择题 下列各电离方程式中,错误的是( )
A.NaOH=Na++O2-+H+
B.Na2SO4=2Na++SO42-
C.HNO3=H++NO3-
D.MgCl2=Mg2++2Cl-
2、实验题 (16分)某学生用0.2000mol・L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作步骤如下:①量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液。
②用标准液滴定至终点,记录滴定管液面读数,所得数据如下表:
| 滴定次数 | 盐酸体积 | NaOH溶液体积读数(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.00 | 18.10 |
| 2 | 20.00 | 0.00 | 16.30 |
| 3 | 20.00 | 0.00 | 16.22 |
3、填空题 A、B代表不同物质,都是H、N、O、Na中的任意三种元素组成的强电解质,A的水溶液呈碱性,B的水溶液呈酸性,请找出A、B可能的两种组合。
要求:相同浓度时,A1溶液中水的电离程度小于A2溶液中水的电离程度;相同浓度时,B1溶液中水的电离程度小于B2溶液中水的电离程度。
(1)写出化学式A1________,A2________,B1________,B2________;
(2)相同温度下,当A1、B1的物质的量浓度相等时,两溶液中水电离出的氢离子的物质的量浓度之比为_______________________;
(3)写出0.1 的A2溶液中离子浓度大小排序 ________________;
(4)B1溶液中水的电离程度小于B2溶液中水的电离程度,原因是 ________________;
(5)若B1、B2两溶液的pH=5,则两溶液中水电离出的氢离子的物质的量浓度之比为__________。
4、选择题 下列电离方程式正确的是
[? ]
A.醋酸溶于水:CH3COOH ==CH3COO-+H+
B.熔融状态下的NaHSO4:NaHSO4==Na++H++SO42-
C.碳酸氢钠溶于水:NaHCO3==HCO3-+Na+
D.硫化氢溶于水:H2S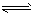 2H++S2-
2H++S2-
5、选择题 下列离子方程式书写正确的是( )
A.向水中通入少量氯气:Cl2+H2O=2H++Cl-+ClO-
B.向硫酸酸化的碘化钾溶液中加入双氧水:2I-+H2O2+2H+=I2+2H2O
C.向氯化铝溶液中加入过量的氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O
D.向碳酸氢钠溶液中加入过量石灰水:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O