时间:2021-02-18 06:42:06
1、填空题 A、B、C、D、E几种常见的化合物或单质之间有如下转化关系: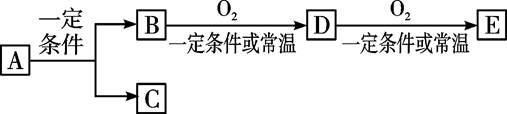
(1)若E是酸酐,D是有刺激性气味的无色气体,则B的化学式是:?;工业上实现D转化为E的化工设备的名称是:?;
(2)若C是酸性气体,B是碱性气体,则E是:?。工业生产实际中合成B选择一定的下列条件的依据是:
①压强?。
②温度?。
(3)若A是日常生活中最常见的物质,C为黄绿色单质气体,则E的电子式为:?;
(4)若A是某有机物,其分子空间构型为正四面体,写出下列反应的化学方程式:
A→B+C:?;
B→D:?。
2、填空题 由短周期元素组成的A、B两种盐可发生下列变化,且B的焰色反应呈黄色。(图中其它生产物未列出)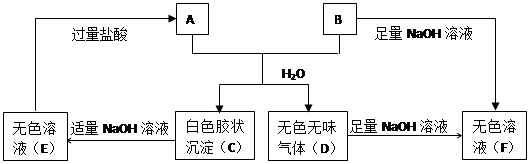
(1)无色溶液(F)中,一定含有的溶质的化学式为?
(2)写出白色胶状沉淀C转化为无色溶液E的化学方程式?
(3)A、E两溶液混合反应时,可观察到的现象是?,写出其反应的离子方程式?
(4)A和B的混合物溶于水发生反应的离子方程式?
3、推断题 甲、乙、丙、丁为4种单质,其中甲、乙、?丙为短周期主族元素的单质,常温下均为气态;丁是日常生活中一种常见的金属。甲、乙、丙、丁生成X、Y、Z、W?四种化合物的转化关系如下:?
甲?+?丙 X?,甲?+?丁
X?,甲?+?丁 Y,丙?+?乙
Y,丙?+?乙 Z?,丁?+?乙
Z?,丁?+?乙 W
W
其中常温下X是无色液体,Y是黑色固体。丙在乙中燃烧发出苍白色火焰,丁在乙中燃烧生成红棕色的烟,W的水溶液呈黄色。
请推断后回答:
(1)写出下列反应的化学方程式:
甲 + 丙 X :___________________
X :___________________
甲 + 丁 Y:___________________
Y:___________________
丙 + 乙 Z :___________________
Z :___________________
丁 + 乙 W:___________________
W:___________________
实验室制取乙物质的化学反应方程式:__________________
(2)已知丙和乙生成Z的过程中,破坏1mol丙的化学键消耗能量Q1kJ,破坏1mol乙的化学键消耗能量Q2 kJ,形成1mol Z的化学键放出能量Q3 kJ。则Q1、Q2、Q3的关系为_________________________。
4、简答题 图中A~H均为中学化学中常见的物质,A、B、H是气体,E是一种白色沉淀,它们之间有如下转化关系.(反应中生成的水已略去)
请回答以下问题:
(1)A是______,C是______,H是______.(填化学式)
(2)干燥的D物质在实验室中常用作______剂.
(3)写出少量B与C反应④的化学方程式:______.
5、简答题 金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G,它们都是中学阶段常见的化学物质,它们之间存在下图所示的转化关系(图中有些反应的产物和反应的条件没有全部标出):
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:丙______,G______.
(2)反应③的化学方程式为______.
(3)反应⑤的离子方程式为______.