时间:2021-02-18 06:22:38
1、实验题 某同学用含硫酸亚铁等杂质的工业硫酸铜制取纯净的氧化铜以探究其性质
(1)制备氧化铜
① 将工业硫酸铜加适量水溶解、搅拌、过滤除去不溶性杂质。简述检验滤液中含有Fe2+的操作方法:____________________________。
② 向滤液中滴加H2O2溶液,稍加热,当Fe2+转化完全后,为将Fe3+全部转化为Fe(OH)3沉淀,而不会将
Cu2+转化为沉淀,需慢慢加入Cu2(OH)2CO3粉末,搅拌,以控制溶液pH=3.5。加热煮沸后过滤,用稀硫酸酸化滤液至pH=1。再从溶液中分离出硫酸铜晶体。Fe2+转化为Fe3+的离子方程式是______________。
③ 在测定所得硫酸铜晶体(CuSO4・xH2O)x值的实验中,所用的玻璃仪器名称为:酒精灯、玻璃棒、_______________,实验过程中称量操作至少进行_______次。
④ 用得到的硫酸铜晶体制氧化铜。
(2)探究氧化铜的性质
在加热条件下,向下图所示装置中持续通入某纯净物X的蒸气,a处黑色物质变为红色, b处白色粉末变为蓝色,c处有无色液体产生。(设各步反应均进行完全) 
则X可能是____________(填一个化学式即可),X与CuO反应的化学方程式是_____________。
参考答案:(1)①取少量滤液于试管中,滴加少量KSCN溶液无现象,再加入少量新制的氯水,溶液呈红色,则证明溶液中含有Fe2+离子。
②2Fe2++H2O2+2H+==2Fe3++2H2O
③干燥器?; 4次
(2)CH3CH2OH ;CH3CH2OH+CuO CH3CHO+H2O+Cu
CH3CHO+H2O+Cu
本题解析:
本题难度:一般
2、实验题 (15分)某校研究性学习小组设计了如图所示装置进行有关实验,实验时将分液漏斗中A逐滴加入烧瓶B中,(图中铁架台、铁夹已略去,要求填写的试剂的均填化学式)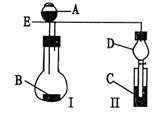
(1)若A为浓硫酸,B为第三周期金属元素的单质,
其在常温下难与水反应;C为品红溶液,实验
观察到C中溶液褪色,则B是?,简述判断B的理由?,
若使C试管溶液恢复原来的颜色,可采取的操作为?。
(2)若B为块状大理石,C为饱和Na2CO3溶液,实验中观察到小试管内溶液变浑浊,则C试管中发生反应的化学方程式为?。
(3)若B是生石灰,实验中观察到C溶液中先形成沉淀,而后沉淀溶解,当溶液恰好澄清时,关闭E,然后将C放入盛有沸水的烧杯中,静止片刻,观察到试管壁上出现光亮银镜。则A是?,C是?与葡萄糖的混合液。仪器D在此实验中的作用是?。
(4)利用此套装置设计实验证明碳酸、醋酸、苯酚的酸性强弱,则A、B、C中放的试剂分别是?、?、?,B、C的实验现象分别为B?、C?。若使现象明显,放入C中的溶液应是稀溶液还是浓溶液?。(填浓或稀)
参考答案:(15分)(1)B是Mg;理由是第三周期元素Na、Mg、Al中①在常温下难与水反应排除Na,②常温下与浓硫酸反应排除Al;加热试管C或放入沸水浴
(2)Na2CO3+CO2+H2O=2NaHCO3↓
(3)A是浓NH3・H2O,C是AgNO3,D是作用是防止倒吸
(4)CH3COOH、NaHCO3、C?6H5ONa;B中有气泡产生,C中溶液变混浊;浓
本题解析:略
本题难度:简单
3、实验题 ?以下是有关SO2、Cl2的性质实验。
(1)某小组设计如图所示的装置图(图中央持和加热装置略去),分别研究SO2和Cl2的性质
①若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同?_______(填“相同”或“不相同”);若装置D中装的是V2O3(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为___________________________。
②SO2通入B中,溶液颜色褪去,则该反应的离子方程式为_______________________。
③E中的试剂为__________(填化学式)。
(2)某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量(填字母)_____________,仍然无法观察到沉淀产生。
A.氨水 B.稀盐酸 C.硝酸钾溶液 D.硫化钠溶液
(3)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4:3;若Cl2与含X的溶液完全反应后,得澄清 溶液,取少量该溶液加入盐酸酸化的氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式_______________________
(4)某科研单位利用电化学原理用SO2来制备硫酸,装置如下图,含有某种催化剂,电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触。通入SO2的电极为____极,其电极反应式为
_________________;电池的总反应式_______________ 
(5)实验是化学研究的基础,关于下列各装置图的叙述正确的是__________。(填序号) 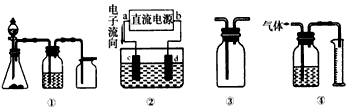
A.装置①可完成多种气体的发生、净化和收集,如铜屑与稀硝酸反应
B.装置②中,a为正极,d为阳极
C.装置③可用于收集H2、NH3、Cl2、HCl、NO2等
D.装置④能用于测量气体体积
(6)用铅蓄电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极)。下列说法中正确的是__________。(填序号) 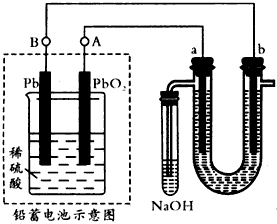
A.铅蓄电池负极的反应式为:Pb -2e-=Pb2+
B.铅蓄电池放电时,B极质量减轻,A极质量增加
C.铅蓄电池充电时,A极应与外电源负极相连
D.电解苦卤水时,a电极首先放电的是Br-
参考答案:(1)①相同;2SO2+O2 2SO3;②SO2+I2+2H2O=4H++2I-+SO42-;③NaOH(其他合理答案也可)
2SO3;②SO2+I2+2H2O=4H++2I-+SO42-;③NaOH(其他合理答案也可)
(2)B
(3)4Cl2+S2O32-+5H2O =2SO42-+8Cl-+10H+
(4)负;SO2-2e-+2H2O=4H++SO42-;2SO2+O2+2H2O=2H2SO4
(5)C
(6)D
本题解析:
本题难度:困难
4、实验题 某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性。 
(1)为完成上述实验,正确的连接顺序为A连____;B连____(填写连接的字母)。
(2)对硬质玻璃管里的氧化铜粉末加热前,需要的操作为_____________
(3)若检验氯气的氧化性,则乙装置的a瓶中溶液可以是____________,对应的现象为____________
(4)丙装置的c瓶中盛放的试剂为___________,作用是________________。
(5)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案精确测量硬质玻璃管的质量为ag,放入
CuO后,精确测量硬质玻璃管和CuO的总质量为b g,实验完毕后。
甲方案:通过精确测量硬质玻璃管和Cu粉的总质量为cg,进而确定Cu的相对原子质量。
乙方案:通过精确测定生成水的质量dg,进而确定Cu的相对原子质量。
①请你分析并回答:________方案测得结果更准确。你认为不合理的方案的不足之处在_________________________
②按测得结果更准确的方案进行计算,Cu的相对原子质量________________
参考答案:(1)E;C
(2)检验氢气的纯度,防止发生爆炸
(3)淀粉KI溶液;溶液变成蓝色
(4)浓硫酸;吸收H2中的H2O
(5)①甲;空气中的CO2和H2O通过D进入U形管造成实验误差较大;②16(c -a)/(b-c)
本题解析:
本题难度:一般
5、选择题 有5种溶液,它们分别是:①KCl;②Ba(NO3)2;③NaOH;④(NH4)2SO4;⑤FeCl3.若要求不用任何外加试剂鉴别它们,则鉴别的先后顺序是( )
A.⑤④①③②
B.⑤③④②①
C.②④③①⑤
D.③②④⑤①
参考答案:铁离子在溶液中显黄色,首先观察溶液的颜色,显黄色的是氯化铁;然后将氯化铁溶液滴入剩余的四种溶液中,一种会出现红褐色沉淀,是氢氧化钠;然后将氢氧化钠溶液滴入剩余三种溶液中,能产生刺激性气体的是硫酸铵;
然后将硫酸铵溶液滴入剩余的两种溶液中出现白色沉淀的是硝酸钡溶液,没有现象的是氯化钾,所以首先根据颜色鉴别出氯化铁,然后根据沉淀的颜色鉴别出氢氧化钠,利用氢氧化钠鉴别出硫酸铵,再利用硫酸铵鉴别出硝酸钡和氯化钾.
故选B.
本题解析:
本题难度:简单