ʱ��:2021-02-18 05:09:16
1��ѡ���� 2014�����绷�����й�����Ϊ������Ⱦ��ս���������йػ�����Ⱦ�������������(?)
A��������Ⱦ��ҪָCO��SO2�����������Լ��۳���
B��������������ɹ⻯ѧ��������Ҫԭ��
C����������ɱ�������������еij�������Խ�ߣ������彡��Խ����
D������ͨ����ָpH��5.6���µĽ�ˮ
�ο��𰸣�C
���������A��������Ⱦ��Ҫָ��������Ķ��˵����������������һ��Σ����CO��SO2�����������Լ��۳������ʲ���Σ�������ʡ���ȷ��B������������������꼰�⻯ѧ��������Ҫԭ����ȷ��C����������ɱ�������������еij��������ϵ�ʱ�����Σ��������̫����˲���һ����Σ��������D�������к���һ����CO2���壬CO2������ˮ���ܽ��γɵı�����Һ��pH=5.6.�������к���SO2��NO2��������ˮ�����γɵ��������ǿ��̼�ᣬ�������H+��ʹ��Һ��pH<5.6.����ͨ��˵��������ָpH��5.6���µ����Խ�ˮ����ȷ��
�����Ѷȣ���
2��ʵ���� ij��ѧС�����Na2SO3������ʵ��̽����
��1���ڰ�ɫ��ΰ��a��b��c���������е���Na2SO3��Һ���ٷֱ�μ���ͼ��ʾ���Լ���
ʵ���������±���
| ��� | ʵ������ |
| a | ��ˮ��ɫ |
| b | ��������ɫ���� |
| c | �����̪��Һ��죬�ټ���BaCl2��Һ����������Һ�ɫ��ȥ |
| ? n(SO32��)�� n(HSO3��) | 91��9 | 1��1 | 9��91 |
| pH | 8.2 | 7.2 | 6.2 |
�ο��𰸣���10�֣�
��1���ٻ�ԭ��?��2�֣�
��SO32-+2S2-+6H+=" 3S��+3" H2O ��2�֣�
����Na2SO3��Һ�У�SO32-ˮ���Լ��ԣ�SO32-+H2O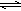 HSO3-+OH-�����Ե����̪����Һ��죻�ڸ���Һ�м���BaCl2��Ba2++SO32-=BaSO3������ɫ��������c(SO32-)��С��SO32-ˮ��ƽ�����ƣ�c(OH-)��С����ɫ��ȥ����2�֣�
HSO3-+OH-�����Ե����̪����Һ��죻�ڸ���Һ�м���BaCl2��Ba2++SO32-=BaSO3������ɫ��������c(SO32-)��С��SO32-ˮ��ƽ�����ƣ�c(OH-)��С����ɫ��ȥ����2�֣�
��2����AC?��2�֣�
��11.2?��2�֣�
�����������1����SO2��Br2��2H2O=H2SO4��2HBr��SO2��S���ϼ����ߣ����������Ի�ԭ�ԣ��𰸣���ԭ��?��2�֣�
�����������£�+4�۵�S��-2�۵�S��Ӧ������0�۵�S,���е���ɫ�������𰸣�SO32-+2S2-+6H+=" 3S��+3" H2O ��2�֣�
��SO32�D����������ӣ�ˮ���ʼ��ԣ���Ba2��ˮ��ƽ�ⱻ�ƻ����𰸣���Na2SO3��Һ�У�SO32-ˮ���Լ��ԣ�SO32-+H2O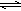 HSO3-+OH-�����Ե����̪����Һ��죻�ڸ���Һ�м���BaCl2��Ba2++SO32-=BaSO3������ɫ��������c(SO32-)��С��SO32-ˮ��ƽ�����ƣ�c(OH-)��С����ɫ��ȥ����2�֣�
HSO3-+OH-�����Ե����̪����Һ��죻�ڸ���Һ�м���BaCl2��Ba2++SO32-=BaSO3������ɫ��������c(SO32-)��С��SO32-ˮ��ƽ�����ƣ�c(OH-)��С����ɫ��ȥ����2�֣�
��2����A��ȷ����Һ�д��ڵ���غ㣬B����ȷ��c(SO32-) > c(HSO3-)��C����ȷ��n(SO32��)�� n(HSO3��)= 91��9ʱ��pH=8.2����Һ�ʼ��ԣ�c(Na+) > c(SO32-)? > c(HSO3-) > c(OH-)>c(H+)����ȷ���ʴ𰸣�AC?��2�֣�
����n(SO32-):n(HSO3-) = 3:2����0.8 mol NaOH��Һ�����˱�״���µ�SO2���������n(SO32-)=3x������Na�� �غ�ã�3x��2��2x=0.8mol,x=0.1mol,n(SO2)=0.5mol,v(SO2?)=0.5mol��22.4l��mol-1=11.2L,�𰸣�11.2?��2�֣�
�����Ѷȣ�����
3��ѡ���� ���й���Ũ�����Ũ�������������ȷ����
A�������¾�����������������
B��¶���ڿ����У���������Һ��������С
C�������¾�����ͭ�Ͽ췴Ӧ
D��¶���ڿ����У���������Һ����������
�ο��𰸣�A
���������Aѡ�����Ũ����Ũ����ۻ������ܹ�ʹ�������������䡣Bѡ�Ũ������������ԣ���Һ�������ӣ�����Cѡ������£�Ũ�����ͭ������Ӧ��Dѡ�Ũ����ӷ�����¶�ڿ����У�������Һ�������١�����
�����Ѷȣ�һ��
4��ѡ���� ���ŵ�ʱ���������м�����������ת��Ϊ����(3O2�ŵ�2O3)������˵����ȷ����(? )
A���˱仯���������仯
B��O2��O3��ͬλ��
C��O2��O3�Dz�ͬ����
D��O2��O3��������ȫ��ͬ
�ο��𰸣�C
�����������ΪO2��O3�ķ�����ɲ�ͬ�����ʲ�ͬ����������ֲ�ͬ�����ʣ���Ϊͬ�������壬���ת��Ϊ��ѧ�仯��
�����Ѷȣ���
5������� �������A��D�ĸ��漰H2O2�ķ�Ӧ(δ��ƽ)����д�հ�
A��Na2O2��HCl����H2O2��NaCl
B��Ag2O��H2O2����Ag+O2��H2O
C��H2O2 H2O��O2
H2O��O2
D��H2O2��Cr2(SO4)3��KOH����K2CrO4��K2SO4��H2O (1)H2O2�����������Եķ�Ӧ��(�����)?��
(1)H2O2�����������Եķ�Ӧ��(�����)?�� (2)H2O2�����������������ֻ�ԭ�Եķ�Ӧ��(�����)?��
(2)H2O2�����������������ֻ�ԭ�Եķ�Ӧ��(�����)?�� (3)H2O2���������Եķ�Ӧ��(�����)?��������Ϊ?��
(3)H2O2���������Եķ�Ӧ��(�����)?��������Ϊ?��
�ο��𰸣�(1)D? (2)C(3)A?��һ��Ӧ�ɿ�����ǿ����ȡ����ķ�Ӧ
��������� ��ӦA��һ����������ԭ��Ӧ��������Ϊ����֪��ǿ�ᣬ����Na2O2��Ӧ��������������õ�H2O2�����ա�ǿ����û����ᡱ�Ĺ��ɣ��ڴ˷�Ӧ��H2O2���ֳ���������ʡ�
��ӦA��һ����������ԭ��Ӧ��������Ϊ����֪��ǿ�ᣬ����Na2O2��Ӧ��������������õ�H2O2�����ա�ǿ����û����ᡱ�Ĺ��ɣ��ڴ˷�Ӧ��H2O2���ֳ���������ʡ� ��ӦB��Ag2O��ɵ��������ɼ�H2O2����һ�ֻ�ԭ�������е���Ԫ��Ӧ��������Ϊת����Ϊ�����������������е�ˮ������Ԫ�ؿ���Ϊ��������������
��ӦB��Ag2O��ɵ��������ɼ�H2O2����һ�ֻ�ԭ�������е���Ԫ��Ӧ��������Ϊת����Ϊ�����������������е�ˮ������Ԫ�ؿ���Ϊ�������������� ��������ķֽⷴӦC����һ������������ԭ��Ӧ��H2O2�ȱ����������ԣ��ֱ����˻�ԭ�ԡ�
��������ķֽⷴӦC����һ������������ԭ��Ӧ��H2O2�ȱ����������ԣ��ֱ����˻�ԭ�ԡ�
�����Ѷȣ�һ��